Поиск и разработка оригинальных лекарственных средств (ЛС) в известном кластере при благоприятном стечении обстоятельств, как правило, занимают15–20 лет. Предопределить сроки открытия инновационных препаратов, тем более инновационных направлений в биологии и медицине невозможно. Не являются исключением в истории медицины случаи, когда у какого-то вещества первоначально открывались одни свойства, а затем другие – дополнительные или даже кардинально меняющие представление о нем как об ЛС. Например, аминазин первоначально был заявлен в качестве антигистаминного средства, затем были открыты его антипсихотические свойства, и он стал основоположником класса нейролептиков. К настоящему времени утрачена уникальность корневого определения фантазийного международного непатентованного названия (МНН) «рацетам», при том что уникальность любого корневого определения МНН заключается, согласно правилам территорий (государств) и Всемирной организации здравоохранения (ВОЗ), в том, что у веществ совпадает сочетание семейственно-групповой химической и классово-групповой терапевтической принадлежности. Общеизвестно, что корневое определение «рацетам» ассоциировано с пирацетамом (ноотропилом).
Пирацетам (ноотропил) по семейственно-групповой химической принадлежности относится к производным пирролидин-2-она группы пирролидина (рис. 1), а по классово-групповой терапевтической принадлежности – к психостимуляторам (психоаналептикам, код АТХ класса: N06) с ноотропным компонентом действия (код АТХ группы N06В/N06ВХ). При этом, например, леветирацетам (кеппра), имея с пирацетамом (ноотропилом) общую семейственно-групповую химическую принадлежность (рис. 1), принципиально отличается от пирацетама по классово-групповой терапевтической принадлежности, характеризуясь диаметрально противоположной направленностью действия. Леветирацетам (код АТХ класса N03; код АТХ группы N03AХ) в отличие от пирацетама принадлежит не к психостимуляторам с ноотропным компонентом действия, а к противоэпилептическим (противосудорожным) лекарственным средствам. Леветирацетам если и обладает, судя по инструкции по применению, влиянием на когнитивную регуляцию, то сугубо негативным, вызывая сонливость, нарушения памяти, мышления, концентрации внимания и амнезию. Его механизм действия связывают с подавлением агонистов ГАМК и возбуждения глутаматных рецепторов, что присуще, например, транквилизаторам, относящимся по семейственно-групповой химической принадлежности к бензодиазепиновому ряду, обладающим противосудорожной активностью и вызывающим амнезию.
Оксирацетам в отличие от пирацетама по семейственно-групповой химической принадлежности принадлежит к производным 4-диагидроксипирролидин-2-она группы 4-диапирролидина (наличие асимметричного атома углерода в 4-м положении молекулярного ядра, указывающего на возможность существования в составе изомерных веществ). Роль и влияние изомерных веществ в составе данного рацемата пока не установлены.
Представленные примеры наглядно демонстрируют следующее: сегодня не известно, что именно представляют собой т. н. рацетамы; далеко не всегда не только потребитель, но и специалист в состоянии разобраться в профессиональной терминологии, тем более когда в терминологию заведомо закладывается дезинформация в отношении устоявшихся представлений (по аналогии и ассоциативных). Пирацетам – это, пожалуй, самый яркий пример в истории медицины, когда препарат, претендуя изначально даже по товарному знаку/оригинальному патентованному названию (ноотропил) на системообразующий класс, не получил такого подтверждения за 40 лет исследований, утратив при этом и уникальность фантазийного корневого определения «рацетам».
Парадокс заключается и в том, что ноотропный эффект пирацетама – не ведущий (родовой/видовой), а ведомый признак (сопутствующий компонент действия), проявляющийся на фоне ведущей психостимулирующей активности в весьма ограниченном диапазоне доз терапевтического окна, что в той или иной мере присуще практически всем психостимуляторам (психоаналептикам). Ноотропный компонент действия пирацетама расслаивается (эксфолиативные признаки компонентов действия) с антигипоксическим эффектом в зависимости от дозы на фоне ведущей активности (Воронина Т.А., 1989). Некоторые препараты, например нейропептиды, обладая более выраженной ноотропной активностью с более широким, чем пирацетам, спектром, вообще не обладают антигипоксическим эффектом, а бензодиазепиновые транквилизаторы, проявляя выраженный антигипоксический эффект, сами вызывают амнезию. Природа ноотропной активности до настоящего времени не установлена. Описанные механизмы действия различных т. н. ноотропов существуют пока на уровне гипотез.

Утрачены иллюзии и относительно безопасности применения т. н. рацетамов. Перечень тяжелейших побочных эффектов леветирацетама – порой с необратимыми последствиями, известных из экспериментальной фармакологии и клинической практики, затмевает собой показания к применению. Необычна схема приема леветирацетама: начинают терапию с достаточно высоких (500 мг), но неэффективных с точки зрения противоэлептического действия доз, постепенно переходя на дозы 1000–1500 мг, определяя, эффективны они или нет в каждом конкретном случае. Навряд ли такой подход оправдан в период эпилептического припадка. Если у пирацетама и леветирацетама есть что-то общее с точки зрения терапевтических признаков, так это необычайно высокий уровень рекомендуемых терапевтических доз, исчисляемых в тысячах миллиграммов, что крайне редкое явление для ЛС.
Пример пирацетама и леветирацетама, иных т. н. рацетамов наглядно демонстрирует чреватость поспешных глобальных выводов, не имеющих специфических критериев оценки того или иного фармакологического эффекта, при этом претендующих на родовое (видовое) определение.
В отношении ноотропной активности канула в Лету, не получив подтверждения, графическая кривая колоколообразной зависимости (доза–эффект) влияния на вызванный транскаллозальный потенциал в качестве критерия специфической ноотропной активности. Не выдерживает критики и отнесение стимуляции нейрометаболизма исключительно к ноотропному эффекту. Во-первых, она связана не только с ноотропным эффектом, а во-вторых, стимуляция чего бы то ни было далеко не всегда может считаться заведомо положительным эффектом.
На модели подпороговых раздражителей у моллюска и в элементарной нейрональной цепи культуры клеток фактически продемонстрирован механизм развития патологии нервной системы и сенсибилизации на фоне дискретной трансмиссии при, казалось бы, ничтожных по силе (физических) и концентрации (химических) методично повторяющихся воздействиях в условиях отсутствия возможности избегания (Кандель Э., 2012). Известно, что эффект пытки каплей воды, выраженный в старинной поговорке «капля камень точит», приводит к сшибке высшей нервной деятельности человека. Образование доминантных форм белков с признаками приона (особый класс инфекционных агентов с аномальной третичной структурой) нарушает нормальную пластичность нервной системы. Преодолевая естественный механизм иммунной реакции и апоптоза, аномальные белки запускают цепную реакцию эпидемии клеточной патологии. Существует гипотеза, будто у низших форм эукариот прионные белки могут являться носителями наследственности и адаптивной регуляции, а у млекопитающих их связывают с распространением ряда нейродегенеративных и иных заболеваний (Зуев В.А. и соавт., 1999).
Метаболизм – слишком обширное понятие, чтобы приписывать его какому-то одному компоненту или даже виду фармакологической активности. Более того, мы показали, что амнезия сама по себе в несколько раз увеличивает плотность рецепторов (включая NMDA), ответственных, как считается, за функциональную регуляцию когнитивных процессов, поэтому вопрос целесообразности их дополнительной стимуляции при амнезии остается открытым [3, 4, 7], а именно модель амнезии и ее упреждение сегодня являются основной методикой определения ноотропного компонента действия в экспериментальной фармакологии. Наши исследования показывают, что упреждение развития и лечение амнезии реализуются не по однотипным механизмам. На необходимость более осторожного подхода к стимуляции нейропластичности через количественное увеличение нейронов и трактовке их увеличения как исключительно положительного феномена указывает также факт химической и клеточной избыточности, например, при аутизме и шизофрении (Аmaral D.G. и соавт., 2008; DiCicco-Bloom E. и соавт., 2006).
В свете открытий, сделанных молекулярными биологами за последние годы [3, 7], не представляется оправданной экстраполяция стимулирующего влияния того или иного ЛС на метаболизм в узком диапазоне доз и тем более в одной дозе на весь терапевтический диапазон его дозировок. Очевидно, что подходы к исследованиям в фармакологии и клинической медицине, сформировавшиеся на базе дихотомии (либо стимуляция, либо подавление – угнетение, торможение, ингибирование) в начале и середине прошлого века, не вполне отвечают современным знаниям в области молекулярной биологии, химизма и электрофизиологии.
Ноотропная и мнемотропная, адаптогенная активности могут иметь место в ряду различных групповых терапевтических признаков различных классов ЛС, т. к. нарушения когнитивной и адаптивной регуляции присутствует в симптомокомплексе практически всех расстройств и болезненных состояний. Они устраняются и компенсируются специфическими по отношению к таким расстройствам и болезненным состояниям препаратами, а никак не пирацетамом и иными психостимуляторами. Совершенно очевидно, что какого-то одного механизма в отношении сложно выстроенной функциональной и патогенетической организации соответствующего элемента когнитивной и адаптивной регуляции нет. Концептуализация ноо- и мнемотропной, адаптогенной активностей как компонентов действия различных классов ЛС приведена нами в соответствие с современными представлениями о сложно организованной полимодальности когнитивной и адаптивной регуляции [3–8].
Сегодня нет ни одного препарата, который бы в полной мере соответствовал понятию ноотропно-функционального и мнемотропно-патогенетического, адаптогенного средства, т. е. имеющего указанные виды активности как ведущие, обеспечивающие проявление других эффектов, восстанавливая при этом любые формы и типы функционально-патогенетических расстройств и патологических состояний когнитивной и адаптивной регуляции. Нет оснований считать пирацетам ноотропным препаратом и родоначальником ноотропной активности как класс-образующей. Пирацетам совершенно обоснованно остается ведущим представителем группы психостимуляторов с ноотропным компонентом действия без ярко выраженного экстенсивного влияния, но и без выраженных терапевтических эффектов невзирая на его применение в дозах, доходящих до 25000–35000 мг/сут и более, при том что его ЛД50 у лабораторных животных составляет 8000 мг/кг. В случае с пирацетамом, очевидно, нарушен постулат определения терапевтического индекса, т. к. он относится не к пищевым, а к лекарственным продуктам.
Сложившаяся практика доказательной медицины показывает, насколько важна экспериментальная фармакология. С ее помощью в относительно короткие сроки выявляются не только те или иные положительные терапевтические эффекты, но и неблагоприятные явления. Более отдаленные и скрытые негативные последствия применения ЛС отслеживать в клинике гораздо сложнее, чем в экспериментальных исследованиях.
Особого внимания при их применении требуют ЛС, имеющие в химической структуре асимметричные атомы, указывающие на возможность существования таких веществ в составе препарата в изомерных формах. Их изучение относится к числу наиболее трудоемких, сложных и дорогостоящих процессов, требующих проведения фундаментальных исследований, разделения изомерных веществ и их получения в стабильном состоянии, изучения их свойств при раздельном применении и в сравнении с рацемическим составом. Асимметричный органический синтез и получение изомерных веществ в стабильном состоянии относятся к числу наиболее сложных химических исследований, требующих от специалистов наивысшей профессиональной подготовки. Обычно определение состава изомеров и их роли в составе ЛС происходит многим позже внедрения таких препаратов в клиническую практику и иногда способно изменить представления о них. Определить состав и свойства изомерных веществ априори и по аналогии пока невозможно.
Так, например, печально известный талидомид был запрещен к применению после того, как уже получил распространение в клинике, вызвав эпидемию рождения детей с физическими уродствами. По разным данным, примерно 40 % (5000 младенцев) из них выжили, оставшись пожизненными инвалидами. До сих пор не известна даже приблизительная статистика в отношении детей, погибших внутриутробно. Определение состава действующих веществ, разделение талидомида на изомеры не решили проблемы тератогенности из-за способности его энантиомеров переходить друг в друга в организме. Ни одно из заявляемых свойств (противосудорожное, седативное, снотворное) талидомида как ЛС не было достоверно подтверждено в исследованиях на животных. Данный пример демонстрирует важнейшую роль доклинических исследований, включая таковые по разным видам эффективности, токсичности и безопасности применения. Сегодня после почти 50-летнего изгнания из медицинской практики талидомид рекомендуется в некоторых странах для лечения проказы, множественной миеломы и иных форм онкологических заболеваний.
Модуляторная и дивергентная концепции (Ахапкина В.И., 2006), включая сопряжение модуляторно-дивергентных отношений в структурно-функциональной-патогенетической организации и управлении организмом, начиная с клеточного уровня [8], базируются на принципе, получившем образное, но отражающее суть название: принцип «балансирующей матрешки» (рис. 2). По этому принципу сформировалась и формируется в процессе эволюции биологическая природа любого организма не без непосредственного влияния окружающей среды обитания, построены не только биологические формы жизни, но и атомы, вещества, галактики и вселенная. Одно и то же вещество, синтезируемое в организме, играет различные роли в зависимости как минимум от места, времени, состояния и концентрации. Концептуализация модуляции (соразмерное влияние) и дивергентности (расхождение влияния) критически относится к принципу дихотомии как к ведущему, на котором базируются устаревшие, но поныне существующие подходы в биологии и медицине, находящие отражение в методических рекомендациях по выявлению и оценке фармакологических эффектов ЛС и их механизмов действия, анатомо-терапевтическо-химической (АТХ) системе классификации ЛС, утвержденных Минздравом и рекомендованных ВОЗ для профилактики и лечения различных расстройств и заболеваний. Концептуализация модуляции и дивергентности в биологии и медицине указывает на их ведущую роль в организации и управлении любым организмом во главе с центральной нервной системой высших животных и человека, где дивергентность – стратегия, модуляция – тактика; стимуляция и подавление – частные и ведомые, регулируемые/недостаточно регулируемые процессы, находящиеся в структуре ведущих.
Ведущая оперативно-тактическая роль модуляции необычайно важна, заключаясь в первую очередь в том, что она то увеличивает, то снижает количество мест сопряжения с дивергентностью. Прошивая (пронизывая) все поле дивергентности (включая места ее сопряжений), она регулирует смену ритмов дивергентности. Находясь во взаимозависимости, влияя друг на друга, модуляция и дивергентность регулируют друг друга и включенные в их структуру стимуляцию, и подавление, тем самым обеспечивая баланс многообразия соотношений протекающих процессов. Стимуляция и подавление сами по себе относительны, поскольку отражают фрагментарное состояние конкретно исследуемого показателя в конкретный момент времени. Приобретение стимуляцией или подавлением относительно устойчивой ведущей роли в каких-то звеньях сопряжения ведущих процессов приводит к развитию расстройств и патологических состояний, старению. Дискретная трансмиссия есть не что иное, как механизм развития патологии. На то же указывает и курсовое применение препаратов с преимущественно однозначно направленной активностью (либо стимуляция, либо ингибирование), приводящей к развитию новых расстройств разной степени тяжести, называемых побочными явлениями. Нередко побочные явления, включая сенсибилизацию, иные злокачественные эпидемиологические процессы, приобретают более тяжелые формы, чем то заболевание, которое лечили тем или иным ЛС. Иногда они становятся необратимыми [7].
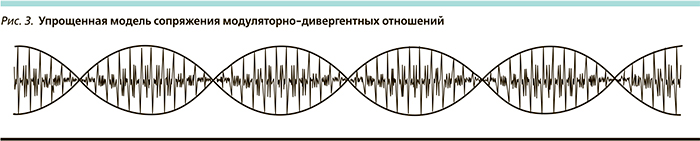
Графическая диаграмма любого исследуемого показателя (гормон, динамичный ген, белок и нейропептид, нейротрансмиттер и т. д.; любая двигательная и исследовательская активность, электрокардиограмма, энцефалограмма) есть не что иное, как модуляция. Зависимость (классически идеализированно – синусоида) характерных и периодически повторяющихся в определенных диапазонах максимумов модуляции – дивергентность. Например, один и тот же нейротрансмиттер, влияя на различные подтипы рецепторов и в различных областях/структурах, будет иметь различные диаграммы модуляции, которые будут сопряжены между собой одновременно полями дивергентности. В абсолютно упрощенной или идеализированной форме (рис. 3) модель модуляторно-дивергентных отношений можно представить в виде двух сопряженных между собой в восьмерки синусоид (дивергентность) с прошивающей их поле (включая места соприкосновений/пересечений) диаграммой (модуляция). Создание модуляторной и дивергентной концепций определяет, что именно и какую роль играет в организме. С точки зрения физики и биофизики волновых процессов дивергентность можно охарактеризовать продольными, а модуляцию – поперечными волнами во всем их многообразии с сопряженными взаимоотношениями.
В фармакологии к дивергентам (расхождение влияния), пусть пока и не вполне совершенным, можно отнести многие известные препараты, изменение направления преимущественного влияния которых на диаметрально противоположное зависит в первую очередь от дозы. Проблема практического подтверждения концептуализации истинной модуляции (соразмерное влияние) в фармакологии заключалась в отсутствии веществ, способных оказывать различное влияние не только по выраженности, но самое главное – по направлению активности в зависимости от состояния организма при разных типах нормы и при разных видах и типах расстройства нормы. Возлагаемые нами надежды на препарат фенотропил, или N-карбамоилметил-4-фенил-2-пирролидон (Патент RU № 2329804 С2 с приоритетом от 28.03.2006), не подтвердились при изучении механизмов действия, включая исследования на субпопуляциях животных с высокой и низкой эффективностью [15, 17, 18], что достаточно полно представлено не только для фенотропила в работе Ю.Ю. Фирстовой [18]. В названия работ хотя и включен термин «модуляция», но в самих примерах исследования, описаниях примеров и выводах говорится исключительно о модулирующем эффекте, т. е. стимулирующем по принципу синергизма и/или опосредованного влияния.
Совокупность стимулирующего синергизма и стимулирующих опосредованных признаков не относится к сугубо специфическим для соразмерного влияния. Это неопровержимо доказано на т. н. иммуномодуляторах – стимуляторах иммунитета, а по аналогии с «иммуномодуляторами» – на т. н. нейромодуляторах [3, 7]. Синергизм и опосредованное влияние относятся к модулирующему влиянию и не несут облигатных критериев истинной модуляции как видовой активности, что сложилось исторически на базе дихотомии. Они имеют место в той или иной степени у всех стимуляторов, включая психо-, иммуно-, инкретостимуляторы и т. д.
Именно поэтому при всей важности противоинсультной активности фенотропила, выявленной на моделях геморрагического и ишемического инсульта, соразмерное влияние не было вынесено нами в формулу изобретения, но все изменилось, когда был не только открыт химический состав фенотропила и тип этого состава [19], но и проведены исследования с хроматографически чистым рацематом и его оптически чистыми энантиомерными веществами [4]. Ранее свойства самого N-карбамоилметил-4-фенил2-пирролидона как такового, влияние на них энантиомерных веществ и их роль в составе рацемата были не известны.
Разработанный нами оригинальный патентованный препарат фенотропил (лабораторное название – карфедон, составленное из слогов химического названия N-карбамоил-метил-4-фенил-2-пирролидон, служившее определенное время названием-легендой, заменявшим шифр, по правилам Института медико-биологических проблем, где начиналась нами разработка препарата) был зарегистрирован в России в 2003 г. в классе психостимуляторов (код АТХ класса: N06) с ноотропной активностью (код АТХ группы N06BХ) с выявленными и описанными для него компонентами действия, указанными в инструкции по применению. Исключительное право по лицензии начиная с 2002 г. предоставлено автором настоящей статьи (непосредственный автор и разработчик препарата от истока и поныне патентообладатель, автор и владелец зарегистрированного оригинального патентованного названия/оriginal brand name – фенотропил, рhenotropilum, рhenotropil и других на национальных языках многих территорий) генеральному партнеру в лице ОАО «Валента Фармацевтика» (Россия) с правом размещения производства фармацевтической субстанции фенотропила на ФГУП СКТБ «Технолог» (Россия). В рамках лицензионного соглашения было передано полностью готовое досье на препарат для освоения производства, проведения регистрации ЛС в виде фармацевтической субстанции и дозированных форм в Минздраве РФ, позволяющих введение препарата в гражданский оборот для практического здравоохранения. Фенотропил после его внедрения в практическое здравоохранение был включен в аптечку международной космической станции (МКС), комплектуемой российской стороной, экспортируется с территории России в другие страны. Это одно из немногих ЛС, которое полностью, включая субстанцию, производится в России.
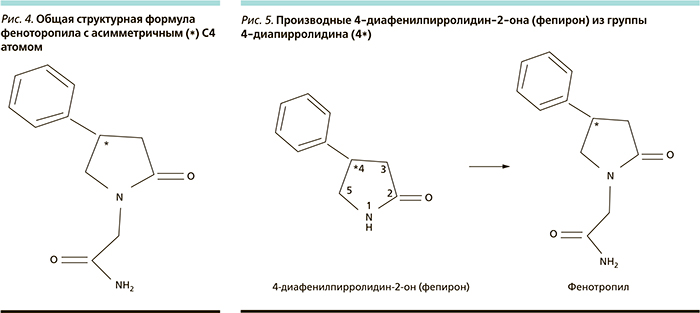
По химической структуре фенотропил (рис. 4, 5) относится к производным (семейство) 4-диафенилпирролидин-2-она (фепирон, 4-фенилпирролидин-2-он, 4-фенилпирролидон) группы 4-диапирролидина (наличие асимметричного атома углерода в положении 4-го молекулярного ядра), что принципиально отличает его от производных пирролидин-2-она группы пирролидина (пирацетам, анирацетам, прамирацетам, леветирацетам; рис. 1). Фепирон, обладая выраженной транквилизирующей (анксиолитической) активностью, не получил клинического применения из-за токсичных свойств. Повреждающим действием на внутренние органы и ткани при наличии той или иной псхотропной активности обладают некоторые ацетилированные и гидроксилированные производные диапирролидинов и пирролидинов.
Диапирролидоны и диапирролидины, пирролидоны и пирролидины широко используются в фармации для получения на их основе ЛС различной терапевтической направленности: от антибиотиков до психотропных средств. Определение семейственно-групповой химической принадлежности веществ в медицине проводится согласно правилам Международного союза теоретической и прикладной химии (ИЮПАК), в первую очередь по структуре их молекулярного ядра и его состоянию (наличие/отсутствие асимметричных атомов) и во вторую – по атомам и группам, непосредственно связанным со скелетом ядра [13, 14, 16]. Присутствие асимметричных центров – наиважнейший признак, непредсказуемо влияющий на свойства веществ. Признаки первой и второй очереди едины и неделимы в определении химической семейственно-групповой принадлежности. Такими признаками для фенотропила являются пятичленный N-гетероцикл с асимметричным С4-атомом, фенильная группа (шестичленный цикл) и атом кислорода в положениях С4 и С2 соответственно (рис. 4). Индивидуальные признаки веществ (группы атомов – боковые цепи, связанные с ядром опосредованно) в определении химической семейственно-групповой принадлежности не участвуют. Приставка «диа» (от гр. dia – через, сквозь; разделение, отделение, промежуточное положение/состояние) сама по себе указывает на наличие асимметричных центров без привязки к их количеству (один и более) и возможность, если не установлено, существования изомерных форм соединения.
Наличие одного асимметричного центра не требует обязательного специального обозначения в органической химии, что не отменяет его очевидного присутствия для специалистов, имеющего важнейшее значение в медицине. История с т. н. рацетамами в медицине показывает назревшую необходимость этого обозначения как обязательного в той или иной общепринятой форме. В медицине четкость и адекватность определений имеют архиважное значение. Они к тому же напрямую связаны с уникальностью корневого определения для МНН ЛС. По сути МНН (INN) являются характерологическим товарным знаком, имеющим значительно большую емкость в гражданском обороте, чем оригинальные патентованные названия. МНН в отличие от последних обычно содержатся в инструкции по применению и представлены на упаковке ЛС без указания рационального химического названия, что при нарушении правил определения их уникальности способно провоцировать введение в заблуждение с непредсказуемыми последствиями.
Бытующие зачастую представления о том, будто фенотропил является производным пирацетама (некий «4-фенилпирацетам») или даже содержит целиком молекулу пирацетама (некий «фенилпирацетам»), что он является производным пирролидин-2-она группы пирролидина (некий «фонтурацетам»), полностью недостоверны. Они вольно или невольно провоцируют введение в заблуждение, в т. ч. ассоциативно. Такие представления обычно связаны либо с отсутствием каких бы то ни было специальных знаний в области органической (в т. ч. фармацевтической) химии, либо с недобросовестностью производителей при наличии таких знаний, либо с узкопрофильной «сленговой» вульгаризацией представлений узким кругом лиц. Последние, употребляя некую «сленговую» терминологию, на самом деле, может быть, и не стремятся ввести в заблуждение или ввести в заблуждение врачей и потребителей, т. к. не занимаются непосредственно промышленным производством и медицинской практикой.
Учитывая, что недостоверные сведения в отношении фенотропила (карфедона) были опубликованы в официальных источниках информации и научных изданиях, приходится их упоминать и на них ссылаться. Однако пришло время расставить все по своим местам, поскольку сегодня они приобретают промышленный размах и международный масштаб. Навязывание дезинформации провоцирует непредсказуемые последствия по объективным или субъективным основаниям, включая ассоциативные, что в отношении ЛС далеко не безобидное занятие. Подобные явления напрямую нарушают законодательные и иные правовые нормы в части получения врачами, фармацевтами и потребителями достоверной информации.
Занимаясь поиском истинных модуляторов для различных терапевтических направлений, мы параллельно вели работы по выявлению роли изомерных веществ в составе фенотропила, т. к. нами был впервые открыт его химический состав и тип рацемата. Материалы были поданы на публикацию в 2005 г. и опубликованы в январе 2006 г. [19]. Рентгеноструктурный анализ выделенных элементарных частиц фенотропила показал, что в кристаллическом состоянии он представляет собой рацемическое соединение. Понятия «рацемическая смесь» и «рацемическое соединение» в органической химии, включая и фармацевтическую химию, не эквивалентны, имеют различные физико-химические характеристики, как правило, различаются по ИК-спектру. Результаты исследования элементарных кристаллических ячеек фенотропила не изменили представлений об иных известных его свойствах и характеристиках, описанных ранее в различных источниках информации.
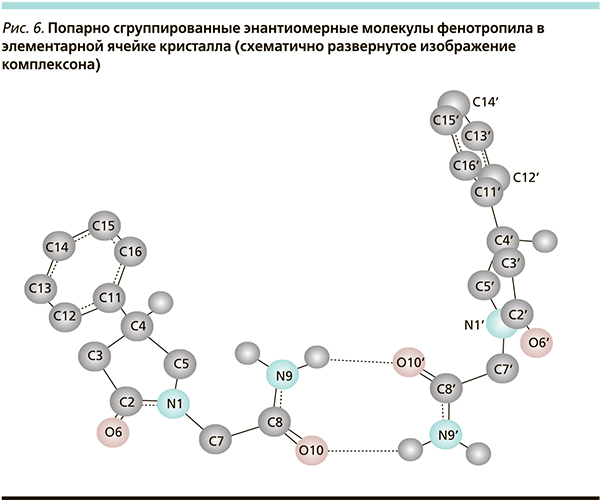
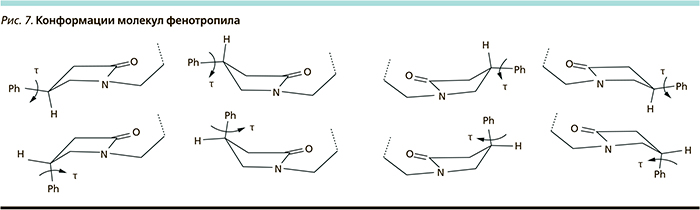
Получение и исследование рацемата в хроматографически чистом состоянии подтвердили, что его стабильность в кристаллическом состоянии обеспечивается комплементарными (образование комплексонов) свойствами [4, 7] за счет достаточно устойчивых межмолекулярных связей между хиральными молекулами, образующими элементарные ячейки (рис. 6). Разрушение этих связей приводит к извращению состава субстанции с утратой стабильности, но для этого необходимо приложить определенные усилия, либо заблокировать другими веществами концевые группы С(О)NH2 в молекулах, либо, разорвав эти связи, «посадить» энантиомерные молекулы на низкомолекулярные или полимерные носители. Никаким иным способом превратить порошок субстанции из рацемического соединения в рацемическую смесь невозможно. Димерные комплексоны хиральных антиподов – молекул фенотропила (рис. 7), представляют собой скрученные ленты, ориентированные вдоль большой диагонали элементарной ячейки. Обнаружены межмолекулярные Н-связи двух типов различной силы. В первом типе межмолекулярных связей участвуют N9–Н(9А)… O10´ и N9´–Н(9´А)… O10. Во втором типе Н-связей участвуют другие атомы водорода групп NН2 и атомы О6, О6´лактамных циклов (на рис. 7 этот тип связей не показан).
Получение и исследование хроматографически чистого N-карбамоилметил-4-фенил-2-пирролидона, его оптически чистых энантиомерных веществ, фармацевтической субстанции рацемата, не имеющей по существу отличий от хроматографически чистого состава, полностью изменили существующее ранее представление о соединении как о химическом веществе (начиная с температуры плавления), так и, что особенно важно, о биологически активном, не имеющем аналогов продукте – ЛС [4]. На примере оригинального инновационного состава (ОИС) фенотропила, или (RS)-2-(2-оксо-4-фенилпирролидин-1-ил)ацетамида, в 2011 г. впервые получила практическое подтверждение и воплощение модуляторная концепция, а сравнительные исследования ОИС фенотропила подтвердили обоснованность дивергентной концепции [1–12].
Выявленными особенностями новизны ОИС фенотропила, или (RS)-2-(2-оксо-4-фенилпирролидин-1-ил)ацетамиды, открывшими его заново для медицины, являются:
- входящие в состав рацемата (R) и (S) вещества обладают выраженной биологической активностью. Не оказывая негативного влияния на физико-химические и биологические свойства рацемата, они уступают ему по рациональной терапевтической эффективности, а в исследованных случаях – и по весьма важным специфическим и сопутствующим компонентам действия;
- температура плавления хроматографически чистого (RS)-2-(2-оксо-4-фенилпирролидин-1-ил)ацетамида составляет 131,0 ± 0,5 – 132,0 ± 0,5 °С (установлено по результатам дериватографических исследований). Температура плавления фармацевтически и фармакологически приемлемой субстанции (совокупное содержание сопутствующих примесей – не более 0,5 %, включая индивидуальные примеси и остаточные количества органических растворителей) – от 130 до 133 °С, а ЛД50 = 1000 мг/кг. Установление ЛД50 выше 1000 мг/кг для данного ЛС нецелесообразно в силу выявленных различий при способе применения, возрастных, половых, видовых и подвидовых особенностей. У крысят из-за малого объема желудка при интрагастральном введении ЛД50 не установлена. Доза 1000 мг/кг при интрагастральном введении не вызывала у крысят токсического влияния с летальным исходом ни в первые, ни в последующие 14 суток наблюдения после введения. Установленные температура плавления и ЛД50 показывают, что сами энантиомерные вещества фенотропила не ухудшают, а улучшают свойства рацемата, повышая уровень токсических доз по сравнению с ранее известным (800 мг/кг), тем самым обеспечивая повышение безопасности применения по терапевтическому индексу (отношение высшей суточной дозы к ЛД50) как минимум на 25,0 %;
- (RS)-2-(2-оксо-4-фенилпирролидин-1-ил)ацетамид обладает модуляторной активностью, проявляющейся избирательно и соразмерно в одних и тех же дозах по направлению и выраженности влияния в зависимости от состояния исследованных функциональных и патогенетических показателей при разных типах нормы и разных видах и типах расстройства нормы, что по облигатным (специфическим) критериям принципиально отличается от влияния дивергентов (расхождение влияния/изменение направления ведущей активности на диаметрально противоположную преимущественно в зависимости от дозы) и препаратов с преимущественно однозначно направленной ведущей активностью, присущей стимуляторам и ингибиторам (подавление, угнетение, торможение). Модуляторная активность с соразмерным влиянием является у ОИС ведущей, определяя его как родоначальника абсолютно нового класса ЛС, основоположника новых фармакотерапевтических направлений и подходов к профилактике, коррекции и лечению различных расстройств и заболеваний;
- соразмерное влияние (RS)-2-(2-оксо-4-фенилпирролидин-1-ил)ацетамида, характеризуясь уни- и промоутмодуляторной активностью, проявляется психо- и психоперандмодуляторными, нейромодуляторными, операндмодуляторными, цитомодуляторными, инкретомодуляторными и иммуномодуляорными компонентами действия;
- уникальная специфичность модуляторной активности (RS)-2-(2-оксо-4-фенилпирролидин-1-ил)ацетамида определяет соразмерный характер таких его выявленных компонентов действия, как нейролептический (антипсихотический), противосудорожный (противоэпилептический), антипаркинсонический, психостимулирующий, анксиолитический, антидепрессивный, ноотропный, мнемотропный, антикревинговый, нейропротекторный, нейротрофический и нейрометаболический, метаботропный и антиапоптозный, анальгезирующий, противоишемический и противоинфарктный (в отношении различных органов и тканей), цереброваскулярный и церебропротекторный, антиоксидантный и прооксидантный, антигипоксический, нормотонический, противоукачивающий, тренинг-стресс-факторный (TSF/Tsf) и адаптогенный эффекты при различных фазах негативного стресса (дистресс и дестресс-дезорганизационная фаза негативного стресса), реювенационный (омолажавающий) и слендерный (похудение без анорексигенного действия) эффекты;
- (RS)-2-(2-оксо-4-фенилпирролидин-1-ил)ацетамид обладает помимо выше перечисленного противовоспалительной, антитоксической, противовирусной, противоканцерогенной, противоульцерогенной, противоотечной, диуретической, регенеративной и репаративной активностью, восстанавливает нарушенную чувствительность рецепторов. Показано, что у животных и человека он восстанавливает фертильные функции, повышает среднюю и максимальную продолжительность жизни у животных. Пилотные исследования в стоматологии ОИС фенотропила (1–25 мг) при острой боли показали, что местное однократное введение в кариозную полость зуба полностью устраняет острую боль и неприятные ощущения через 3–15 минут с сохранением эффекта не менее 48 часов без ограничения приема пищи и воды, режима гигиенической чистки зубов. Обезболивающий эффект ОИС, как показали исследования, многофункционален при введении в организм, местном введении и наружном применении;
- (RS)-2-(2-оксо-4-фенилпирролидин-1-ил)ацетамид не имеет ограничений по способам применения, что определено при введении в организм, местном введении и наружном применении животными и человеком, не имеет ограничений в зависимости от пола и возраста. Отсутствие наркогенной активности, отсутствие развития привыкания и зависимости, наличие соразмерно-реверсивной и антикревинговой активности не ограничивают его курсовое применение любой целесообразной длительности;
- пороговая биологически активная доза при введении в организм снизилась как минимум в 3 раза и составляет 1 мг/кг для животных. При местном введении и наружном применении порог биологически активных и терапевтических доз у животных и человека существенно снижается по сравнению с дозами для внутрибрюшинного, внутривенного и интрагастального введения (в среднем при разведении последних 1 : 100). ОИС не требует изменения терапевтических разовых и суточных доз для человека по сравнению с ранее известными при введении в организм, но их специфика и выраженность влияния, безопасность применения средства принципиально отличаются от ранее известного для препарата. Эффективные терапевтические дозы не требуют коррекции для половозрелых, стареющих и старых животных. Токсические и терапевтически эффективные дозы для крысят 30–35-дневного возраста даже несколько выше, чем для половозрелых животных, но при этом, как установлено, дозы и экспозиции самих повреждающих факторов (химических и физических агентов) для достижения уровня моделируемой патологии у неполовозрелых животных тоже выше, чем у половозрелых. Эти исследования показали, что детский организм более устойчив к некоторым агрессивным факторам, чем взрослый;
- выявлены триггерные и реверсивные свойства, способность энантиомеров переходить друг в друга в организме и биологических средах организма. Электронографические исследования в газовой среде показали наличие изменения пространственной изомерии. Выявлено как минимум 4 стабильных конформационных состояния не только для рацемата, но и для каждого энантиомера при раздельном исследовании. Конформационные особенности в значительной степени определяют физические, химические и биологические свойства веществ. Установить переходные состояния и их влияние экспериментальными методами невозможно, а исключать их влияние на организм у данного препарата нет оснований.
Свойства энантиомеров существенно осложняют их получение в стабильном состоянии раздельно и затрудняют их исследования, при этом указывая на наличие мутаротации за счет перераспределения электронной плотности в молекулах (таутомерия). Получение энантиомерных веществ в стабильном состоянии – наисложнейший процесс, в десятки раз превосходит по стоимости рацемат, требует применения стабилизаторов. Механическое смешивание энантиомеров и их рацемизация сопровождаются резким падением температуры плавления. Результаты проведенных исследований указывают на то, что для энантиомерных веществ фенотропила большое значение имеют не только высокие, средние, но и низкие виды энергии. Известно, что таутомерия играет большую роль в химии циклических и гетероциклических карбонильных соединений, синтезируемых и трансформируемых в организме. Разные формы и типы изомерии в различных условиях не только устанавливают, но и сдвигают равновесие. Среда обитания и ее состояние оказывают существенное влияние на пространственную ориентацию атомов в молекулах, на комплементарные (образование комплексонов по механизму «ключ–замок») и комплиментарные (от комплимент – прием, перенос и отдача ионов) свойства веществ.
Учитывая, что (RS)-2-(2-оксо-4-фенилпирролидин-1-ил)ацетамид практически не метаболизируется в организме, объяснить его уникальную ведущую специфическую активность, спектр выявленных специфических и сопутствующих компонентов действия во всем его многообразии можно только изомерией и стереоспецифичностью, способностью веществ проявлять комплементарные и комплиментарные свойства, усиливать и снижать в зависимости от состояния распространение волновых процессов, включая симметричные и асимметричные электрофизиологические.
Исследования в области структурной химии ОИС фенотропила и его изомеров продолжаются, поэтому пока рано делать какие-то окончательные выводы, конкретизировать роль той или иной изомерной формы и типов изомерии в привязке к тем или иным выявленным компонентам специфической фармакологической активности и сопутствующим эффектам. Структурные исследования, как и любые другие, требуют неоднократного их воспроизведения по разным методологиям. Тем ни менее полученные результаты исследований в области структурной химии, в экспериментальной и клинической фармакологии с не известной ранее ведущей базовой активностью, беспрецедентно широким спектром специфических и сопутствующих компонентов действия (выявленных в подавляющем большинстве случаев впервые) указывают на то, что (RS)-2-(2-оксо-4-фенилпирролидин-1-ил)ацетамид фактически действует не как два вещества в одном составе, а как большее число веществ из димерного состава хиральных антиподов. Наличие у молекул фенотропила асимметричного атома углерода в пятичленном ядре, фенильной группы, атома кислорода, углерод-углеродных связей линейной группы ацетамида с концевой С(О)NH2 группой, водорода в положении С4 представляют большой интерес для исследований в области структурной химии и молекулярной биологии.
У нас есть основания полагать, что скорость трансформаций энантиомерных молекул фенотропила неодинакова в биологических средах.
Рацемат фенотропила (кристаллический порошок белого цвета, реже – со слегка кремоватым оттенком) мало- растворим в воде и физиологическом растворе, что не позволяет проведение его исследований в обычных стандартных лекарственных формах без применения специальных процедур. При нагревании или, например, применении Твина 80 растворимость фенотропила резко повышается. Стабильность подогретых растворов при хранении в обычных условиях не превышает двух часов в зависимости от температуры нагрева. Поддержание температуры стандартных растворов на уровне 36,6–37,0 оС, физиологичном для человека, увеличивает срок их стабильности. Выход температуры плавления фармацевтического состава субстанции (RS)-2-(2-оксо-4-фенилпирролидин-1-ил)ацетамида за пределы границ от 130 до 133 оС по начальной и конечной точкам плавления прямо указывает на высокую степень загрязненности состава примесями. Согласно данным дериватографического и капиллярного методов исследования, температура плавления фармацевтически приемлемой субстанции ОИС от начальной до конечной точки укладывается в границы 0,2–0,9 оС, составляя в среднем 0,5 ± 0,055 оС. Для рацематов и иных комплексных составов лекарств в отличие от единичных веществ нецелесообразно устанавливать стандарт температуры плавления только по конечной точке.
Индивидуальные сопроводительные примеси (исходный и промежуточные продукты синтеза) фенотропила в основном хиральны, биологически высокоактивны, способны не только маскировать, но и извращать физико-химические, биологические и фармакотерапевтические свойства действующего состава. Большую роль в фармацевтическом составе субстанции играют и остаточные количества органических растворителей. В сочетании с индивидуальными примесями они способны вызывать полиморфизм субстанции, сокращая сроки и ограничивая условия хранения по температурному режиму. Достижение указанной выше чистоты фармацевтической субстанции при содержании действующего соединения не менее 99,0 % и не более 100,5 % (определено наиболее точным титриметрическим методом со стандартной ошибкой метода, не превышающей обычно 5,0 %, т. е. ± 0,5) в пересчете на сухое вещество и при потере в массе при высушивании не более 0,1 % приводит к полному соответствию показателей фармакологической активности, присущих хроматографически чистому составу. Государственная Фармакопея также указывает на преимущество титриметрического метода как наиболее точного. Показатели количественного определения методом ВЭЖХ (высокоэффективная жидкостная хроматография) и СВЭЖХ (сверхвысокоэффективная жидкостная хроматография) должны быть подтверждены титриметрическим методом, т. к. стандартная ошибка количественного определения достигает 20 %, т. е. ± 2,0 в абсолютном исчислении.
Идентификация и количественное содержание индивидуальных примесей в фармацевтической субстанции проводятся методом ВЭЖХ или СВЭЖХ. В зависимости от способа получения перечень сопроводительных индивидуальных примесей может меняться, но изменение их суммарного количественного содержания в % не должно превышать установленного показателя. Метод тонкослойной хроматографии способен ввести в заблуждение относительно состава примесей, их идентификации, количественного содержания. При оценке потери в массе при высушивании не требуется определения содержания воды (в данном случае не более 0,5 %) и наоборот. Корреляция количественного содержания сопроводительных примесей, как идентифицированных, так и не идентифицированных с наиболее точно установленным количественным содержанием действующего соединения, гарантирует его выявленную эффективность.
Хроматографически чистый ОИС фенотропила и его разработанный фармацевтически и фармакологически приемлемый состав субстанции стабильны как минимум 5 лет в условиях хранения при температуре не выше 30 °С. Метод ускоренного старения не выявил полиморфизма субстанции при сроке хранения, соответствующем 3 годам. Следовательно, восстановление комплементарных отношений между энантиомерными молекулами, приводящих к стабилизации состава, происходит достаточно быстро при условии, что состав не отягощен и не извращен присутствием других веществ.
Учитывая то обстоятельство, что ранее препарат (ЛД50 = 800 мг/кг) был заявлен, зарегистрирован и в настоящее время широко применяется как ноотропное средство, а ноотропная активность официально приписана в существующей АТХ-системе классификации к классу психоаналептиков (психостимуляторов), необходимо специально подчеркнуть следующее: ноотропная активность ОИС фенотропила является для него не ведущей, а одним из компонентов действия, который, проистекая из модуляторной активности, принципиально отличается от такового у психостимуляторов, включая пирацетам. Необходимо отметить и то, что ОИС фенотропила как модулятор с соразмерным влиянием может в любом случае заменить собой психостимулятор пирацетам и другие психостимуляторы. Он эффективнее и рациональнее в применении, многоплановость его эффектов саморегулируется через соразмерную реверсивность и триггерную трансмиссию в пределах модуляции, увеличивая или сокращая места сопряжений с дивергентностью (играющей ведущую стратегическую роль в организме), тем самым оказывая прямое влияние на ее состояние. Пирацетам как средство выбора заменить собой ОИС фенотропила не может ни по ведущей активности, ни по компонентам действия, включая ноотропный. Проявляющийся иногда у фенотропила в разовых терапевтических дозах отчетливый дивергентный эффект связан либо с истощением энергетического потенциала организма, либо с хроническим извращением фаз дивергентности. Это в свою очередь указывает на то, что эффекты фенотропила способны затрагивать не только оперативно-тактические модуляторные процессы, но и сугубо дивергентные процессы, связанные со стратегической ролью смены парадигмы в границах гомеостатической норы биоритмологии патогенеза. Подобные эффекты фенотропила указывают направления поиска истинных дивергентов.
Проистекая из ведущей модуляторной активности, ноотропный компонент действия ОИС, как, впрочем, и психостимулирующий, соразмерен, что установлено по влиянию на вызванный транскаллозальный потенциал, мнестические функции (память, внимание, обучение) и исследовательское поведение, при обучении и амнезии в субпопуляциях высоко- и низкоэффективных половозрелых животных, а также крысят 30–35 дневного возраста. Механизмы действия (RS)-2-(2-оксо-4-фенилпирролидин-1-ил)ацетамида по показателям nАCh, NMDA, BDNF, подтипам дофаминовых и бензодиазепиновых рецепторов также соразмерны в субпопуляциях, имея существенные различия. Механизмы действа ОИС фенотропила различаются в условиях нормы (при ее разных типах) и в условиях разных видов и типов расстройства нормы и форм патологии, что не присуще стимуляторам и ингибиторам с преимущественно однозначно направленной активностью.
Ранее существенным ограничением для применения фенотропила являлось не только присутствие в настоящем, но и наличие у пациентов в прошлом эпизодов манифестации панических атак и иных форм психомоторного возбуждения. ОИС проявляет выраженный и уникальный нейролептический (антипсихотический) эффект при позитивной (гиперактивация дофаминергической системы) и негативной (гиперактивация серотонинергической системы) симптоматике шизофрении, при гиперактивации М-холинергической системы как звена патогенеза психозов, превосходя по многим позициям эффекты оланзапина в сравнительных исследованиях [3, 4, 7, 12], а также проявляя терапевтическую эффективность там, где оланзапин оказался неэффективным. Дополнительных исследований требуют взаимоотношения фенотропила с серотонинергической системой. Не исключено, что при серотонинергической патологии его эффективные дозы могут быть гораздо ниже, чем при дофаминергической.
Противосудорожная активность ОИС не ограничена моделями, указывающими на отсутствие эффективности, и побочными явлениями, присущими, например, леветирацетаму и бензодиазепиновым транквилизаторам. Антикревинговая активность препарата может найти место при лечении различных форм зависимости. Ранее предполагалось ограничение применения фенотропила не только при гиперактивном состоянии ЦНС, но и при гиперактивности иммунной и гормональной систем, при анорексии, артериальной гипертензии. ОИС фенотропила в определенной степени устраняет эти препятствия. Слендерная активность ОИС, способствующая нормализации массы тела, не связана с анорексигенным эффектом. Анорексигенная активность у ОИС отсутствует. Устранены препятствия к применению высоких терапевтических доз фенотропила по экстренным показаниям за счет существенного изменения его терапевтического индекса, позволяющего обеспечивать достаточную безопасность данного ЛС в таких случаях, как инсульт, тяжелые формы черепно-мозговых травм и иные острые поражения головного мозга. Противоинсультная активность ОИС более выраженна, обеспечена большей безопасностью применения, курсовое применение не ограничено стимулирующим или ингибирующим эффектом в силу наличия соразмерно реверсивной модуляторной активности. Учитывая, что в эксперименте фенотропил предотвращает развитие инфаркта, оказывает лечебный эффект при инфаркте не только тканей головного мозга, требуются более углубленные исследования препарата при инфаркте тканей различных органов, включая сердце и почки.
Патент RU № 2480214 С1 на изобретение «Состав, обладающий модуляторной активностью с соразмерным влиянием, фармацевтическая субстанция (варианты), применение фармацевтической субстанции, фармацевтическая и парафармацевтическая композиция (варианты), способ получения фармацевтических составов» с приоритетом от 22.09.2011 не просто поглощает собой Патент RU № 2050851 С1 («Вещество, проявляющее ноотропную активность», с приоритетом от 28.08.1990), Патент RU № 2232578 С1 («Вещество, обладающее антидепрессивной активностью», с приоритетом от 10.04.2003 и его подтвержденный правовой международный статус), Патент RU № 2329804 С2 («Вещество, обладающее нейротропной – нейромодуляторной активностью», с приоритетом от 28.03.2006 и его подтвержденный международный правовой статус по противоинсультной активности – лечение геморрагического и ишемического инсульта) и любые иные ранее известные патенты, касающиеся в той или иной степени N-карбамоилметил-4-фенил-2-пирролидона, но впервые открывает его истинные свойства и характеристики с определением роли и значения рацемата для медицины по инновационной специфической ведущей активности, ее специфическим и сопутствующим компонентам действия, роли входящих в его состав действующих веществ, полностью изменив представление о них. Он открывает не известные ранее в биологии и медицине перспективы профилактики, коррекции и лечения различных расстройств и заболеваний функционального, патогенетического, смешанного и биполярного характера.
Открытие истинных свойств и характеристик фенотропила и как N-карбамоилметил-4-фенил-2-пирролидона, и как (RS)-2-(2-оксо-4-фенилпирролидин-1-ил)ацетамида или с любым иным достоверным для него химическим названием также позволило впервые идентифицировать и квалифицировать существенные недостатки (пороки) ранее известной продукции на основе данного соединения, не только полученной нами, но и воспроизводимой другими авторами, заявителями и производителями.
Так, например, пороком изобретения SU № 797219, A61 K21/40 – «N-карбамоилметил-4-фенил-2-пирролидон, обладающий гипотензивной активностью» (приоритет от 08.05.1979, дата публикации 25.07.1995) является то, что на самом деле в нем описан не N-карбамоилметил-4-фенил-2-пирролидон. На что прямо указывают сочетание температуры плавления 132 оС с ЛД50 = 831 мг/кг, характеристика соединения как продукта конденсации пирацетама и 4-фенилпирролидона-2, описание картины токсического влияния и летальность при введении токсических доз мышам. Для специалистов очевидно, что при конденсации пирацетама и 4-фенилпирролидона-2 (см. определение реакции конденсации) можно получить более сложное соединение из двух указанных более простых в описании к SU № 797219, A61 K21/40, но никак не N-карбамоилметил-4-фенил-2-пирролидон или 1-карбамоилметил-4-фенил-2-пирролидон, указанные в тексте описания изобретения. Учитывая, что половина авторов (включая первого) SU № 797219, A61 K21/40 – профессиональные химики, нет никаких оснований признать случайным или ошибочным такое весьма характерное специально подчеркнутое указание в описании изобретения. Данное изобретение до настоящего времени не получило промышленного применения, поэтому так и осталось неизвестно, что именно в нем исследовано, описано и заявлено.
Пороком продукции «Карфедона Фармакопейного» из МУК 4.1.234-96 (Москва, 2000, действие продлено в 2004 г.) является то, что в ней 1-карбамоилметил-4-фенилпирро-лидон-2 обладает желтым цветом и имеет температуру плавления 130–140 оС. Рассчитать весь аналитический ряд (от «как минимум» и до «как максимум») по количественному содержанию 1-карбамоилметил-4-фенилпирролидона-2 в продукции для специалиста не составляет труда в соответствии с нормативами Государственной Фармакопеи, если не указано иного. В данном случае самый химически грязный фармацевтический состав субстанции с содержанием заявленного действующего соединения как минимум имеет температуру плавления 130 оС, а самый чистый – 139–140 оС, что абсолютно недостоверно для данного соединения.
Олайнфарм (Латвия), пытаясь воспроизвести оригинальный препарат фенотропил производства «Валента Фармацевтика» (Россия), зарегистрированный, в т. ч. на Украине, неправомерно полностью переписав инструкцию по применению оригинального препарата, добился в итоге того, что энтроп (N-карбамоилметил-4-фенил-2-пирролидон) не влияет на физическую трудоспособность (Компендиум – лекарственные препараты, 2007–2011). Отсутствие влияния на физическую трудоспособность полностью исключает вероятность того, что действующим соединением в энтропе является N-карбамоилметил-4-фенил-2-пирролидон или только N-карбамоилметил-4-фенил-2-пирролидон. Данный порок исключает применение по указанным показаниям и приписку препарата к психостимуляторам-ноотропам. Отсутствие влияния на физическую трудоспособность полностью исключает какую бы то ни было аналогию с фенотропилом (карфедоном). Прием фенотропила, как известно, лишил медали лыжницу Ольгу Пылеву на олимпийских играх в Турине (2006). Фенотропил (карфедон) входит в перечень препаратов, запрещенных для спортсменов в период спортивных соревнований, именно из-за высокой активности в отношении физической трудоспособности. То, что соответствующие зарубежные ведомства с нарушением авторских и патентных прав смогли зарегистрировать энтроп для практического здравоохранения в качестве эквивалентного фенотропилу аналога, не имеет научно-практического и правомерного в рамках законодательства объяснения.
Полиморфизм субстанции энтропа, начинающийся при температуре нескольким выше 15 оС (хранение таблеток при температуре не выше 15–25 оС), является дополнительным тому подтверждением. Устранение порока отсутствия влияния на физическую трудоспособность у энтропа (фенилпирцетама) с внесением изменений в его инструкцию по применению (Компендиум – лекарственные препараты, 2012 и 2013 гг., внесение изменений в инструкцию на энтроп – зарегистрировано Минздравом Украины 10.09.2011) привело к тому, что он приобрел иной дополнительный порок: не рекомендуется принимать препарат при вождении транспортных средств и управлении иными механизмами, что уже вступает в антагонистические противоречия с заявленной для него ноотропной активностью. Полиморфизм действующего соединения не устранен. Производитель должен доказать заведомо недоказуемое – наличие в действующем составе у энтропа молекулы пирацетама, т. к. в название-синоним одного препарата (фенилпирацетам) целиком включено название другого (пирацетам). N-карбамоилметил-4-фенил-2-пирролидон не содержит и даже теоретически не может содержать молекулу пирацетама. Он априори не может быть производным (семейственная принадлежность) пирацетама. Пирацетам вообще не является и по определению не может быть родоначальником химической группы каких бы то ни было ЛС и химических веществ.
Энтроп не только не избавился от известных теперь недостатков продукции на основе N-карбамоилметил-4-фенил-2-пирролидона, но и приобрел дополнительные пороки. Энтроп не эквивалентен не только ОИС фенотропила, но и ранее известной продукции фенотропила на основе N-карбамоилметил-4-фенил-2-пирролидона.
Причину извращения состава энтропа и субстанции N-карбамоилметил-4-фенил-2-пирролидона можно объяснить описанием из EP 2013166 B1 (приоритет от 16.03.2006) и WO 2007/104780 А2 (дата публикации 20.07.2007 – заявитель Олайнфарм, Латвия) на примере некоего т. н. карфедона. Его пороком является то, что он, согласно описанию, извращен до состояния рацемической смеси, а входящий в состав рацемической смеси «(S)/(-)-карфедон» существенно ухудшает его фармацевтические и биологические свойства, что специально подчеркнуто в выводах описания изобретения. Чтобы извратить карфедон до состояния рацемической смеси, необходимо, как теперь известно, блокировать достаточно выраженную комплементарную активность его энантиомерных веществ другими (посторонними) веществами, поэтому, что именно исследовалось и с чем проводились сравнительные исследования, осталось и, вероятно, останется не известно. Судя по температуре плавления 107,5–108,0 оС, указанной для «R/(+)-карфедона», не указанной для «(S)/(-)-карфедона» и «карфедона», а в таких случаях (если не указано иного) принято считать идентичным указанному, тем более что проводились сравнительные исследования, информация только подтверждает, что это не карфедон и не его энантиомерные вещества. Отсутствие ЛД50 указывает на его идентичность ранее известному, но судя по температуре плавления это невозможно.
Каких-либо фармакологических свойств в EP 2013166 B1 и WO 2007/104780 А2, не известных ранее по направлению влияния для фенотропила (карфедона), и фармакологических свойств для т. н. энантиомеров, не известных ранее для фенотропила (карфедона), не показано. Показано, что «карфедон» и его энантиомеры в дозах 100 мк/кг обладают однотипной, но в разной степени выраженной стимулирующей – антидеприссивной – активностью по методике Porlsot; стимулируют в дозах 50 мг/кг локомоторную (двигательную) активность вертикального и горизонтального компонентов и практически не влияют на исследовательское поведение по методике открытого поля; энантиомеры в одинаковой и гораздо более высокой дозе по ЕД50 вызывают миорелаксацию и обезболивающий эффект (метод горячей пластины). Явное расхождение базовой активности в зависимости от дозы присуще дивергентам. Отсутствие контрольных исследований в таблице, посвященной исключительно энантиомерным веществам, не позволяет говорить о достоверности результатов и отличии их от контроля. Сам факт наличия исследуемых эффектов не установлен. Дозы выше 500 и ниже 50 мг/кг, как это указано в таблице, не применялись, что подтверждено подстрочником к таблице. Название таблицы не соответствует показателям и описанию.
Данные источники информации напрямую касаются по формуле изобретения только (R)/(+)-энантиомера, но, поскольку в примерах описания присутствует рацемат, мы были вынуждены их анализировать. При этом получить указанным в п. 7 формулы EP 2013166 B1 и WO 2007/104780 А2 способом само вещество по п. 1 со свойствами п.п. 1–5 невозможно. Способом синтеза в любом случае можно получить некое техническое сырье, но никак не требуемое вещество или требуемый состав веществ, не говоря уж о изомерах данного рацемата. Очистка колончатой хроматографией в описании примеров промышленно неприменима. Под модуляцией (п. 4 формулы) авторы и заявитель понимают стимулирующий синергизм двигательной (локомоторной) активности, что к модуляции как к таковой (соразмерное влияние) не имеет специфического отношения. Психическое возбуждение, как известно, всегда сопровождается повышением двигательной активности. Пункт 1 формулы также неправомерен, поскольку понятие «нейротропная активность» – общее, как и само понятие «нервная система», т. е. не подлежащее патентной защите.
Однотипно отмечается выраженное расхождение компонентов действия (эксфолиативные признаки) у энантиомеров без выявленной в данном случае ведущей у них и у рацемата активности и указывающей на возможность их отнесения к явным дивергентам. Учитывая, что ни в одном из примеров не указан растворитель, под ним необходимо понимать дистиллированную воду, но фактически карфедон в воде и физиологическом растворе настолько малорастворим, что исследования провести невозможно, поэтому в данном случае информация в отношении стандартной лекарственной формы недостоверна. Что именно исследовалось и описано в данных источниках информации, неизвестно. Судя по характеристикам это не N-carbamoylmethyl-4-phenyl-2-pyrrolidinon, не N-carbamoylmethyl-4(R)-phenyl-2-pyrrolidinon и не N-carbamoylmethyl-4(S)-phenyl-2-pyrrolidinon.
По истечении нескольким более 4 лет авторами EP 2013166 B1 и WO 2007/104780 А2 (Zvejniece L., Svalbe B., Veinberg G., Grinberga S., Vorona M., Kalvinsh I., Dambrova M.: Investigation into stereoselective pharmacological activity of phenotropil. Basic Clin Pharmacol Toxicol 2011;109(5):407–12. doi: 10.1111/j.1742-7843.2011.00742.x. Epub 2011 Jul 20) представлены материалы исследования якобы фенотропила и якобы энантиомеров фенотропила. Однако т. н. фенотропил и его энантиомеры не имеют отличий от т. н. карфедона (рацемическая смесь) и его энантиомеров из описания EP 2013166 B1 и WO 2007/104780 А2, т. к. иного и отличного от них ни по физико-химическим, ни по фармакологическим свойствам не указано. Кроме того, эффекты всех без исключения препаратов существенно ухудшились, что прямо вытекает при анализе и сопоставлении представленной в этих источниках информации результатов исследования. Уточнены явно дивергентные свойства в зависимости от дозы энантиомеров и рацемата. Препараты исследовались в стандартной композиции с физиологическим раствором, но фенотропил настолько малорастворим в нем, что провести его исследование в стандартной композиции с физиологическим раствором так же невозможно, как и в стандартных водных растворах. Различий, подтверждающих подлинность указанных энантиомеров и рацемата не представлено, а если не указано иного, то необходимо понимать как ранее известное.
Также следует указать, что полностью недостоверна информация ВОЗ [WHO Drug Information 2009;23(2); 2010;24(1)] в отношении некоего «fonturacetamum» («fonturacetam», «fonturacetam»), или rac-2-[(4R)-2-oxo-4-phenylpirrolidin-1-yl]ацетамида. Такой препарат нигде на территориях не был зарегистрирован, поэтому, чья это текущая и притом недостоверная версия, не известно. Аналогия с пирацетамом по семейственно-групповой химической принадлежности в данном случае не просто неуместна, но и недостоверна. Указанный рацемат не является по аналогии с пирацетамом производным пирролидидона группы пирролидина, что достаточно подробно изложено выше и продемонстрировано на рис. 1 и 4–6. Недостоверна она и в отношении того, что рацемат (rac) содержит биологически инертное (S)-энантиомерное вещество. На что прямо указывает выведение его за пределы состава ЛС в рациональном химическом названии rac-2-[(4R)-2-oxo-4-phenylpirrolidin-1-yl]ацетамид, а также характеристика в описании: «ноотропный агент и энантиомер».
В таких случаях (если по всем позициям доклинических исследований действительно доказано отсутствие у одного из веществ в составе какой бы то ни было положительной и негативной биологической активности) действующее вещество необходимо указывать в ½ части от рацемата. То есть если рацемата взято 100 мг, то эффективная доза энантиомерного вещества в ЛС должна указываться исключительно как 50 мг.
Изменение химического названия с rac-2-[(4R)-2-oxo-4-phenylpirrolidin-1-yl]ацетамид на название, содержащее в составе (S)-энантиомера [WHO Drug Information 2022;25(1)], ничего, по существу, для «fonturacetamum» («fonturacetam») не изменило, подтвердив отсутствие у составителей рекомендации достоверной информации в отношении фармакологических свойств и семейственно-групповой химической принадлежности веществ данного рацемата и его самого. Информация и рекомендация ВОЗ в данном случае если и могут иметь место, то исключительно в качестве сугубо нарицательного примера.
Исключение из правил при присвоении МНН, как показывает практика и описано в представленных выше примерах, приводит к вульгаризации корневого признака МНН, утрате им уникальности (единство семейственно-групповой химической и классово-групповой терапевтической принадлежности веществ).
В случае промышленного применения подобных МНН любой потребитель вправе предъявить производителю и регистрирующему государственному органу претензию по объективным и субъективным основаниям, в любом случае неопровержимым с точки зрения правовых законодательных норм. Это касается любого МНН, несущего заведомо недостоверную информацию. Ушли в прошлое времена, когда потребитель был не осведомлен о своих правах или лишен прав на получение достоверной информации. В западных странах немалое число лиц превратили в своеобразный бизнес недомыслие производителей и безбедно существуют, выигрывая судебные процессы в подавляющем большинстве случаев совершенно обоснованно. Упрекнуть в чем-то потребителей нет никаких оснований, поскольку производители сами заложили дезинформацию в свою продукцию и инструкцию по ее применению, что и привело к неблагоприятным для них последствиям.
Существенным недостатком композиции RU 2183117 C1 (приоритет от 03.11.2000, заявитель «АСЛГ Исследовательские лаборатории») является отсутствие иных сведений о ранее известном в отношении действующего соединения. При этом для достижения желаемого эффекта с целью нормализации артериального давления и лечения гипертонической болезни (в 58 % случаях как максимум) требуется курсовое применение N-карбамоилметил-4-фенил-2-пирролидона в чрезмерно высоких дозах (750 мг/сут в 3 приема, «но предпочтительнее принимать однократно»). Рекомендуемые эффективные курсовые дозы составляют 1000 мг 1–4 раза в сутки, что превышает известное на тот период ЛД50 = 800 мг/кг у мышей, а иного не указано. Индекс безопасности не обеспечен. Ближайшими аналогами продукции N-карбамоилметил-4-фенил-2-пирролидона являются, судя по нозологической принадлежности и исследованиях с участием человека, «Карфедон Фармакопейный» из МУК 4.1.234-96 (Москва, 2000) и состав из SU № 797219, A61 K21/40, пороки которых описаны ниже, а иного, за исключением эффективных доз, не указано. Изобретение полностью опровергает наличие гипотензивной активности у соединения в качестве специфической. Клинические исследования были остановлены, изобретение не получило промышленного применения. АСЛГ «Исследовательские лаборатории» пыталось улучшить свойства известного им т. н. Карфедона Фармакопейного за счет составления биологически активной композиции с включением в ее состав фармацевтической субстанции 1-(4-фенил-2-пирролидон)ацетамида, янтарной, яблочной или другой двух- или трехосновной органической кислоты (Патент RU 2192858 С1 с приоритетом от 16.05.2001), что в итоге привело к содержанию посторонних примесей на уровне 6,0 %. В процессе ускоренного старения количественное содержание активных компонентов сокращалось на 10 %, а содержание посторонних примесей, соответственно, возрастало до 16 %. Данные факты исключают саму возможность практического применения такой композиции. Известно, что указанные кислоты обладают влиянием на метаболизм, гипотензивной, антигипоксической, адаптогенной, нейротропной, кардиотропной и противоишемической/кардиотропной активностью. Аналогичный состав известен из заявки на изобретение 199900877 (Бюллетень Евразийского патентного ведомства 1-2001, 26.02.2001), применение которого ограничено pH и низкой биодоступностью.
Существенным недостатком композиции из Патента RU № 2240783 С1 (приоритет от 17.07.2003), обладающей ноотропной активностью, и способа ее получения является то, что при заявлении ноотропной активности как ведущей в составе к тому же содержится 0,5 % нехарактерной (неродственной) сопроводительной примеси (2-пирролидон), которая в полном смысле посторонняя и не может присутствовать в фармацевтическом составе. Совокупное содержание индивидуальных сопроводительных примесей увеличивается в разы, причем они не идентифицированы. Каких-либо иных новых, не известных ранее свойств не выявлено.
Существенным недостатком композиции из Патента RU № 2327458 С1 (приоритет от 19.02.2007) является то, что состав в заявленной композиции нестабилен при хранении, содержание примесей увеличивается, что непредсказуемо для эффективности; каких-либо иных, не известных ранее свойств не выявлено. Применение чрезвычайно ограничено по способу введения, неприемлемо для педиатрии из-за присутствия этилового спирта. Токсичность продукции повышается.
Существенным недостатком фармацевтической композиции из RU 2414898 C1 (приоритет от 18.09.2009), обладающей ноотропной активностью, является то, что при снижении количества действующего рацемата при хранении композиции психостимулирующая активность увеличивается по сравнению с раствором субстанции. Следовательно, увеличивается количество неидентифицированных примесей со стимулирующей активностью, конкурирующих в организме за места связывания. Исключить стимулирующий синергизм основного действующего соединения и примесей нет оснований. Изобретение не получило промышленного применения, каких-либо иных, не известных ранее свойств не выявлено.
Существенным недостатком фармацевтического состава из WO 2009/048352 А1 (приоритет от 12.10.2007) при высокодисперсной микронизации является адгезия молекул Н2O молекулами соединения, извращающая свойства субстанции, образуя устойчивую взвесь.
К каждой молекуле энанатиомера достаточно прочно присоединяются молекулы воды, замыкая их по ацетамидной группе в замок, фармакологическая активность резко снижается, промышленное применение нецелесообразно; каких-либо иных, не известных ранее свойств не выявлено.
Существенным недостатком фармацевтического состава в виде микроинкапсулированных поликомпонентных частиц из N-карбамоил-метил-4-фенил-2-пирролидона (Патенте RU 2391976 с приоритетом от 18. 10. 2007) является то, что масса субстанции увеличивается за счет присутствия дополнительного компонента. Состав нестабилен, биологические свойства ухудшаются, промышленное применение нецелесообразно, каких-либо иных, не известных ранее свойств не выявлено.
Имеется упоминание «фенилпирацетама» (карфедона) в преамбуле описания изобретения US 2009/0306225 А1 (дата публикации – 10.12.2009, приоритет 21.04.2009) наряду еще с 15 т. н. рацетамами, включая псисохстимулятор пирацетам и противоэпелептическое (противосудорожное) средство леветирацетам. Последний фармакологически активен не сам, а за счет вторичного метаболита. Каких-либо примеров исследования ни для одного из т. н. рацетамов не представлено, каких-либо свойств т. н. рацетамов также не представлено и не описано. Представлены примеры исследования разработанных композиций, являющихся предметом изобретения формулы, с известными противовоспалительными средствами и подобранными для них вспомогательными веществами и носителями для их введения специальным шприцем в лабиринт среднего уха.
При этом предполагается, что для всех 16 указанных т. н. рацетамов такая композиция в указанных диапазонах концентраций с перечнем представленных вспомогательных веществ и носителей и в указанных пропорциях компонентов полностью идентична невзирая на различия в их физико-химических свойствах, включая растворимость и т. д. Все они, несмотря на то что леветирацетам подавляет стимуляцию глутаматных рецепторов головного мозга, при введении в лабиринт среднего уха должны, по мнению авторов и заявителя, вопреки здравому смыслу стимулировать глутаматные рецепторы головного мозга и опосредованно стимулировать иммунитет, обеспечивая лечебный эффект. Невозможно представить, каким образом будет метаболизироваться в лабиринте среднего уха леветирацетам, чтобы проникнуть в головной мозг, преодолев гематоэнцефаллический барьер, превратившись при этом из подавляющего глутаматные рецепторы средства в стимулирующее.
Источник информации US 2009/0306225 А1 не имеет никакого отношения к ОИС фенотропила и фенотропилу в целом, но он приведен в качестве примера упоминания «фенилпирацетама» («карфедона») как ассоциативного заблуждения даже среди профильных специалистов в отношении т. н. рацетамов и примера сквотеринга, противоречащего законодательству, но широко практикуемого вопреки законодательству в некоторых странах. Медицинские области относятся к числу сугубо доказательных и строго регламентированных, в которых аналогия не уместна, а если и имеет место, то исключительно по результатам сравнительных экспериментальных и клинических исследований.
Таким образом, представленные материалы и их анализ показывают, что свойства и характеристики N-карбамоилметил-4-фенил-2-пирролидона, или (RS)-2-(2-оксо-4-фенилпирролидин-1-ил)ацетамида, роль входящих в его состав энантиомерных веществ были не известны, впервые были открыты и описаны нами в 2011 г. [4]. Установлено, что все без исключения ранее существовавшие описания касались не самого соединения, а в лучшем случае – продукции на его основе и то с весьма различными свойствами и характеристиками, зачастую вступающими в антагонистические противоречия друг с другом.
Впервые в истории медицины получено синтетическое средство, обладающее модуляторной активностью, соразмерное влияние которого по направлению и выраженности напрямую зависит от состояния организма при разных типах нормы, разных видах и типах расстройств нормы, способное при этом преодолевать специализацию различных клеток и тканей, а также реверсироваться в зависимости от состояния среды обитания исходно и в процессе изменения ее состояния с проявлением соразмерной триггерной трансмиссии механизмов действия. Модуляторная активность, модуляция, модуляторы приобрели в биологии и медицине совершенное иное и, что самое главное, объективное и доказанное на конкретных примерах значение.
Благодаря ОИС фенотропила и сравнительным с его применением исследованиям полностью подтверждены два абсолютно новых базовых явления: модуляторное (соразмерное влияние) и дивергентное (расхождение влияния), что открывает перспективные направления в науке и практике. Открытие ведущей специфической активности у ОИС фенотропила, подтверждение при сравнительных исследованиях модуляторной и дивергентной концепций требуют введения в АТХ-классификацию новых классов со специфическими для них облигатными критериями и систематизацией их групп и подгрупп.
Разработанный в свое время специалистами ВОЗ рациональный подход в АТХ-классификации ЛС позволяет не ломать, а расширять ее рамки, дополняя новыми классами, сохраняя исторически сложившуюся преемственность, подчеркивая при этом появляющиеся инновационные направления. Например, среди нейротропных классов модуляторы с собственными облигатными критериями, систематизацией их групп и подгрупп могут занять позицию N08, а дивергенты – N09. Подобное расширение классов модуляторов и дивергентов, судя по выявленным эффектам ОИС фенотропила, легко вписывается в любые АТХ-системы, включая как функциональные, так и патогенетические.
Мы далеки от мысли, что нам удалось получить идеальный модулятор, но то что на примере ОИС фенотропила и с его помощью заложена новая фундаментальная основа, имеющая большое значение для практической медицине, не вызывает сомнений. Не исключено, что в скором времени модуляторы и дивергенты появятся в различных АТХ-системах.
Новые поколения инновационных средств из числа модуляторов и дивергентов будут способны преодолевать доминантную химическую и клеточную патологию, приводящую к различным функциональным и патогенетическим расстройствам и заболеваниям, включая злокачественные новообразования, сенсибилизацию, развитие различных форм зависимости. Они изменят представление о профилактике старения, будут способны преодолевать мутации патогенных микроорганизмов и вирусов без вредоносного влияния на организм.
Фармакологические исследования и исследования молекулярных механизмов действия ОИС фенотропила достаточно наглядно демонстрируют подобные возможности модуляторов с соразмерным влиянием.



