1. Введение
Настоящие рекомендации по диагностике и лечению больных болезнью Крона (БК) разработаны экспертной комиссией ООО «Ассоциация гастроэнтерологов России», ООО «Ассоциация колопроктологов России» и Общества по изучению воспалительных заболеваний кишечника (ВЗК) при Ассоциации колопроктологов России в составе: Ивашкин В.Т., Шелыгин Ю.А., Абдулганиева Д.И., Абдулхаков Р.А., Алексеева О.П., Барановский А.Ю., Белоусова Е.А., Головенко О.В., Григорьев Е.Г., Костенко Н.В., Низов А.А., Николаева Н.Н., Осипенко М.Ф., Павленко В.В., Парфенов А.И., Полуэкто-ва Е.А., Румянцев В.Г., Тимербулатов В.М., Ткачев А.В., Халиф И.Л., Хубезов Д.А., Чашкова Е.Ю., Шифрин О.С., Щукина О.Б.
В работе над рекомендациями принимали также участие: Алексеенко С.А., Болихов К.В., Валуйских Е.Ю., Головенко А.О., Григорьева Г.А., Жигалова Т.Н., Князев О.В., Куляпин А.В., Лахин А.В., Михайлова Т.Л., Морозова Н.А., Никитина Н.В., Никулина И.В., Одинцова А.Х., Светлова И.О., Ситкин С.И., Соловьев О.Л., Ткаченко Е.И., Юрков М.Ю., Яков-лев А.А.
Рекомендации составлены на основании данных литературы, Европейского доказательного консенсуса по диагностике и лечению БК, представленного Европейским обществом по изучению язвенного колита и болезни Крона (ECCO), и включают следующие разделы: определение и классификация БК, диагностика, консервативное и хирургическое лечение, прогноз.
Для отдельных положений рекомендаций приведены уровни доказательности (УД) и согласно общепринятой классификации Оксфордского Центра доказательной медицины. Библиография включает 102 российских и зарубежных источника, однако в настоящей публикации рекомендации приводятся без списка литературы. Рекомендации являются руководством для практических врачей при ведении пациентов с БК и подлежат регулярному пересмотру в соответствии с новыми данными научных исследований в этой области.
1.1. Валидизация рекомендаций
Настоящие рекомендации в предварительной версии были рецензированы независимыми экспертами, которых попросили прокомментировать прежде всего то, насколько интерпретация доказательств, лежащих в основе рекомендаций, доступна для понимания. Получены комментарии со стороны врачей амбулаторного звена, которые тщательно систематизировались и обсуждались на совещаниях экспертной группы.
Последние изменения в настоящих рекомендациях были представлены для дискуссии на заседании профильной комиссии «Колопроктология» Экспертного совета Минздрава России 17 декабря 2012 г. Проект рекомендаций был повторно рецензирован независимыми экспертами и врачами амбулаторного звена. Для окончательной редакции и контроля качества рекомендации были повторно проанализированы членами экспертной группы, которые пришли к заключению, что все замечания и комментарии приняты во внимание, риск систематических ошибок при разработке рекомендаций сведен к минимуму.
2. Определение и классификация болезни Крона
2.1. Определения
Болезнь Крона – хроническое, рецидивирующее заболевание желудочно-кишечного тракта (ЖКТ) неясной этиологии, характеризующееся трансмуральным, сегментарным, гранулематозным воспалением с развитием местных и системных осложнений. При БК могут поражаться любые отделы ЖКТ – от полости рта до ануса. В большинстве случаев БК поражает илеоцекальный отдел. В отличие от язвенного колита (ЯК) БК не может быть излечена ни терапевтическими, ни хирургическими методами.
Обострение (рецидив, атака) БК – появление типичных симптомов заболевания в стадии клинической ремиссии, спонтанной или медикаментозно поддерживаемой.
Ремиссия БК – исчезновение типичных проявлений заболевания (УД 5, СР D). Выделяют:
- клиническую – отсутствие симптомов БК (соответствует значению индекса активности БК < 150; см. ниже);
- эндоскопическую – отсутствие видимых макроскопических признаков воспаления при эндоскопическом исследовании;
- гистологическую ремиссии – отсутствие микроскопических признаков воспаления.
2.2. Классификация БК
Для описания локализации поражения применяется Монреальская классификация (табл. 1). Поражение верхних отделов ЖКТ редко встречается в изолированном виде и, как правило, дополняет терминальный илеит, колит или илеоколит.
I. По распространенности поражения выделяют:
локализованную БК:
- c поражением протяженностью менее 30 см. Термин обычно используют при изолированном поражении илеоцекальной зоны (< 30 см подвздошной кишки + правый отдел толстой кишки);
- возможно изолированное поражение небольшого участка толстой кишки;
распространенную БК – поражение протяженностью более 100 см (сумма всех пораженных участков).
II. По характеру течения выделяют:
острое течение (менее 6 месяцев от дебюта заболевания):
- c фульминантным началом;
- c постепенным началом;
хроническое непрерывное течение (отсутствие ремиссии в течение 6 месяцев от начала обострения на фоне адекватной терапии);
хроническое рецидивирующее течение:
- редко рецидивирующее (обострения 1 раз в год или реже);
- часто рецидивирующее (2 обострения и более в год).
III. По тяжести заболевания
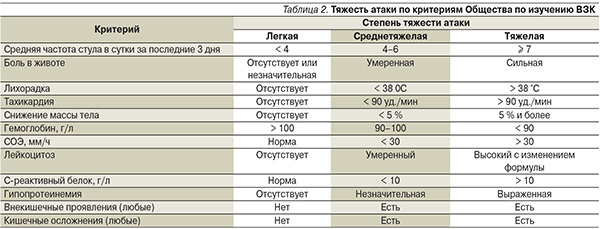
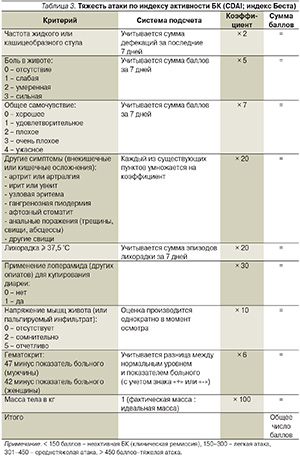
Тяжесть заболевания в целом определяется тяжестью текущей атаки, наличием внекишечных проявлений и осложнений, рефрактерностью к лечению, в частности развитием гормональной зависимости и резистентности. Однако для формулирования диагноза и определения тактики лечения следует определять тяжесть текущего обострения (атаки; УД 1b, СР В), для чего используются простые критерии, разработанные Обществом по изучению ВЗК при Ассоциации колопроктологов России, и индекс активности БК (ИАБК; индекс Беста, СDAI), как правило, применяемый в клинических испытаниях ввиду сложности его расчета. Выделяют легкую, среднетяжелую и тяжелую атаки БК (табл. 2, 3).
IV. По фенотипическому варианту БК подразделяют на (Монреаль, 2005):
нестриктурирующий, непенетрирующий тип (просветный или воспалительный);
стриктурирующий тип (стенозирующий);
пенетрирующий тип (свищевой).
Перианальные поражения (свищи, анальные трещины, перианальные абсцессы) могут дополнять любой из указанных фенотипических вариантов.
V. По ответу на гормональную терапию как для БК, так и для ЯК выделяют:
гормональную резистентность:
- в случае тяжелой атаки – сохранение активности заболевания, несмотря на в/в введение глюкокортикостероидов (ГКС) в дозе, эквивалентной 2 мг/кг/сут, в течение более 7 дней;
- в случае среднетяжелого обострения – сохранение активности заболевания при пероральном приеме ГКС в дозе, эквивалентной преднизолону 0,75 мг/кг/сут, в течение 4 недель;
гормональную зависимость:
- увеличение активности болезни при уменьшении дозы ГКС ниже дозы, эквивалентной преднизолону 10–15 мг/сут, в течение 3 месяцев от начала лечения;
- возникновение рецидива болезни в течение 3 месяцев после окончания лечения ГКС.
2.3. Формулировка диагноза
При формулировании диагноза следует отразить локализацию поражения с перечислением пораженных сегментов ЖКТ, характер течения заболевания, фазу течения (ремиссию или обострение), тяжесть текущей атаки или наличие ремиссии, наличие гормональной зависимости или резистентности, а также наличие внекишечных проявлений или кишечных и перианальных осложнений (см. раздел «Диагностика»).
3. Диагностика болезни Крона
3.1. Клинические диагностические критерии БК
К наиболее частым клиническим симптомам БК относятся:
- диарея, в т. ч. с кровью;
- боль в животе;
- потеря массы тела;
- лихорадка;
- анемия;
- пальпируемый инфильтрат брюшной полости;
- аноректальные поражения (трещины, свищи, парапроктит);
- внекишечные проявления (табл. 4).
К числу кишечных осложнении БК относятся:
- наружные свищи (кишечно-кожные);
- внутренние свищи (межкишечные, кишечно-пузырные, ректо-вагинальные);
- инфильтрат брюшной полости;
- межкишечные или интраабдоминальные абсцессы;
- стриктуры ЖКТ;
- кишечная непроходимость;
- анальные трещины;
- парапроктит (при аноректальном поражении);
- кишечное кровотечение.
3.2. Установление диагноза БК
Диагноз БК ставится на основании сочетания данных анамнеза, клинической картины и типичных эндоскопических и гистологических изменений.
Необходимо учитывать следующие данные:
- данные, полученные при подробном опросе пациента (характер начала заболевания, поездки в южные страны, непереносимость пищевых продуктов, прием лекарственных препаратов, включая антибиотики и нестероидные противовоспалительные средства, наличие аппендэктомии в анамнезе, курение, семейные заболевания);
- детальный физикальный осмотр (УД 1b, СР B), включая осмотр перианальной области, пальцевое исследование прямой кишки, ректороманоскопия (УД 5, СР D);
- обзорная рентгенография брюшной полости (при симптомах кишечной непроходимости (УД 5, СР D);
- тотальная колоноскопия с илеоскопией (УД 5, СР D);
- фиброгастродуоденоскопия (УД 3a, СР C);
- рентгенологическое исследование пассажа бариевой взвеси по тонкой кишке (после исключения признаков непроходимости; УД 5, СР D);
- биопсия слизистой оболочки кишки в зоне поражения при эндоскопии (УД 5, СР D);
- ультразвуковое исследование (УЗИ) органов брюшной полости, забрюшинного пространства, малого таза (УД 5, СР D);
- трансректальное УЗИ прямой кишки и анального канала (при перианальных поражениях; УД 5, СР D);
- исключение острой кишечной инфекции, паразитарного колита, псевдомембранозного колита;
- исследование крови (общий анализ крови, СОЭ, С-реактивный белок, коагулограмма, биохимический анализ крови, группа крови и резус фактор; УД 2b, СР B).
Диагноз должен быть подтвержден: эндоскопическим и морфологическим методом и/или эндоскопическим и рентгенологическим методом.
При необходимости проводят следующие дополнительные исследования:
- магнитно-резонансную (МРТ) и компьютерную томографию (КТ) для диагностики свищей, абсцессов, инфильтратов;
- фистулографию (при наличии наружных свищей);
- капсульную эндоскопию (при подозрении на поражение тонкой кишки и в отсутствие стриктур). Следует помнить, что задержка капсулы в кишечнике наблюдается у 13 % пациентов. В настоящее время больным БК до проведения капсульной эндоскопии рекомендуется выполнять рентгенологические исследования (пассаж бариевой взвеси по кишечнику, КТ-энтерография) или МРТ-энтерографию для оценки наличия стриктур тонкой кишки;
- баллонную энтероскопию (при подозрении на поражение тонкой кишки).
Общепринятыми являются критерии достоверного диагноза БК по Lennard–Jones, включающие определение следующих признаков заболевания:
 Поражение от полости рта до анального канала: хроническое гранулематозное поражение слизистой оболочки губ или щек; пилородуоденальное поражение, поражение тонкой кишки, хроническое перианальное поражение.
Поражение от полости рта до анального канала: хроническое гранулематозное поражение слизистой оболочки губ или щек; пилородуоденальное поражение, поражение тонкой кишки, хроническое перианальное поражение.
Прерывистый характер поражения.
Трансмуральный характер поражения: язвы–трещины, абсцессы, свищи.
Фиброз: стриктуры.
Лимфоидная ткань (гистология): афтоидные язвы или трансмуральные лимфоидные скопления.
Муцин (гистология): нормальное содержание муцина в зоне активного воспаления слизистой оболочки толстой кишки.
Наличие саркоидной гранулемы.
Диагноз БК считается достоверным при наличии 3 любых признаков или при обнаружении гранулемы в сочетании с любым другим признаком.
Эндоскопическими критериями диагностики БК являются регионарное (прерывистое) поражение слизистой оболочки, симптом «булыжной мостовой» (сочетание глубоких продольно ориентированных язв и поперечно направленных язв c островками отечной гиперемированной слизистой оболочкой), линейные язвы (язвы-трещины), афты, а в некоторых случаях – стриктуры и устья свищей.
Рентгенологические проявления БК включают регионарное, прерывистое поражение, стриктуры, «булыжную мостовую», свищи и межкишечные или интраабдоминальные абсцессы.
- Морфологическими признаками БК служат:
- глубокие щелевидные язвы, проникающие в подслизистую основу или мышечный слой;
- саркоидные гранулемы (скопления эпителиоидных гистиоцитов без очагов некроза и гигантских клеток), которые обычно обнаруживаются в стенке резецированного участка и только в 15–36 % случаев – при биопсии слизистой оболочки;
- фокальная (дискретная) лимфоплазмоцитарная инфильтрация собственной пластинки слизистой оболочки;
- трансмуральная воспалительная инфильтрация с лимфоидной гиперплазией во всех слоях кишечной стенки;
- поражение подвздошной кишки со структурными изменениями ворсин, мукоидной или псевдопилорической метаплазией крипт и хроническим активным воспалением;
- прерывистое поражение – чередование пораженных и здоровых участков кишки (при исследовании резецированного участка кишки).
В отличие от ЯК крипт-абсцессы при БК формируются редко, а секреция слизи остается нормальной.
3.3. Дифференциальный диагноз
Дифференциальный диагноз БК проводят с:
- язвенным колитом;
- острыми кишечными инфекциями *: дизентерией, сальмонеллезом, кампилобактериозом, иерсиниозом, амебиазом;
- глистными инвазиями;
- паразитозами;
- антибиотико-ассоциированными поражениями кишечника (C. difficile);
- туберкулезом кишечника;
- системным васкулитом;
- неоплазиями толстой и тонкой кишки;
- дивертикулитом;
- аппендицитом;
- эндометриозом;
- солитарной язвой прямой кишки;
- ишемическим колитом;
- актиномикозом;
- лучевыми поражениями кишечника;
- синдромом раздраженного кишечника.
4. Консервативное лечение болезни Крона
4.1. Принципы терапии
Выбор вида консервативного или хирургического лечения определяется тяжестью атаки, протяженностью и локализацией поражения ЖКТ, наличием внекишечных проявлений и кишечных осложнений (стриктуры, абсцесса, инфильтрата), длительностью анамнеза, эффективностью и безопасностью ранее проводившейся терапии, а также риском развития осложнений БК.
Целями лечения БК являются индукция ремиссии и ее поддержание без ГКС, профилактика осложнений и операций. Хирургическое лечение не приводит к полному излечению пациентов даже при удалении всех пораженных сегментов кишечника, поэтому необходима противорецидивная терапия, которую следует начинать не позднее 2 недель после операции.
Следует особо отметить, что ГКС не могут применяться в качестве поддерживающей терапии.
4.2. БК илеоцекальной локализации (терминальный илеит, илеоколит), легкая атака
Приоритетной считается терапия первой линии будесонидом 9 мг/сут в течение 8 недель, затем – снижение дозы по 3 мг в неделю до полной отмены (УД 2a, СР B). В случае достижения ремиссии поддерживающая терапия проводится месалазином (УД 5, СР D).
Для индукции ремиссии возможно назначение месалазина (4 г/сут), однако убедительных доказательств возможности применения месалазина как препарата первой линии не получено, хотя мета-анализ 3 крупных исследований продемонстрировал статистически значимое превосходство 5-аминосалициловой кислоты над плацебо. Терапевтический эффект при лечении месалазином (отсутствие симптомов, ИАБК ≤ 150) следует оценить через 4 недели. При достижении ремиссии прием месалазина в прежней дозе пролонгируется до 8 недель, для поддержания ремиссии также используется месалазин.
В отсутствие терапевтического ответа на любой из указанных препаратов дальнейшее лечение проводится, как при среднетяжелой атаке БК.
4.3. БК илеоцекальной локализации (терминальный илеит, илеоколит), среднетяжелая атака
Показана терапия ГКС в сочетании с иммуносупрессорами: для индукции ремиссии применяются будесонид
(9 мг/сут; УД 1a, СР A) или пероральные ГКС (преднизолон 1 мг/кг или метилпреднизолон 0,8 мг/кг; УД 1a, СР A). Решение о применении системных ГКС (а не топического ГКС будесонида) принимается с учетом выраженности системных проявлений БК. Наличие внекишечных проявлений и/или инфильтрата брюшной полости диктует выбор системных ГКС. Одновременно назначаются иммуносупрессоры: азатиоприн (АЗА; 2 мг/кг), 6-меркаптопурин (6-МП; 1,5 мг/кг), а при непереносимости тиопуринов – метотрексат (25 мг/нед подкожно или внутримышечно). Эффект от терапии ГКС оценивается в течение 1–3 недель. Терапию полной дозой ГКС не следует проводить более 1–3 недель. При достижении клинической ремиссии (ИАБК < 150) на фоне продолжения терапии иммуносупрессорами проводится снижение дозы ГКС до полной отмены: преднизолон – снижение по 5–10 мг в неделю; метилпреднизолон – по 4–8 мг в неделю; будесонид – прием 9 мг/сут в течение 8 недель, затем снижение по 3 мг в неделю. Суммарная продолжительность терапии ГКС не должна превышать 12 недель. Поддерживающая терапия иммуносупрессорами проводится не менее 4 лет (УД 1a, СР A). В отсутствие эффекта от ГКС или при обострении БК после отмены/снижения дозы ГКС (гормонозависимая форма) или неэффективности терапии иммуносупрессорами (рецидив через 3–6 месяцев после отмены ГКС) показана биологическая терапия (инфликсимаб, адалимумаб) или хирургическое лечение (УД 1b, СР A). Поддерживающая терапия после достижения ремиссии при помощи биологической терапии проводится инфликсимабом/адалимумабом в комбинации с иммуносупрессорами. Тактика противорецидивной терапии после хирургического лечения описана в разделе 5.5. «Противорецидивная терапия после хирургического лечения БК».
4.4. БК толстой кишки, легкая атака
Лечение легкой атаки БК толстой кишки может эффективно проводиться при помощи перорального сульфасалазина в дозе 4 г или перорального месалазина в дозе 4 г (УД 1b, СР A).
Оценка терапевтического эффекта выполняется через 2–4 недели. При достижении клинической ремиссии (ИАКБ ≤ 150) поддерживающая терапия проводится также сульфасалазином или месалазином 4 г (не менее 4 лет). В отсутствие терапевтического ответа лечение проводится, как при среднетяжелой атаке БК (УД 1a, СР B).
4.5. БК толстой кишки, среднетяжелая атака
Показана терапия системными ГКС в сочетании с иммуносупрессорами: для индукции ремиссии применяются преднизолон 1 мг/кг или метилпреднизолон 0,8 мг/кг (УД 1a, СР A). Одновременно назначаются иммуносупрессоры: АЗА (2 мг/кг), 6-МП (1,5 мг/кг), а при непереносимости тиопуринов – метотрексат (25 мг/нед подкожно или внутримышечно). Эффект от терапии ГКС оценивается в течение 1–3 недель. Терапию полной дозой ГКС не следует проводить более 1–3 недель. По достижении клинической ремиссии (ИАБК < 150) на фоне продолжения терапии иммуносупрессорами проводится снижение дозы ГКС до полной отмены: преднизолон – снижение по 5–10 мг в неделю, метилпреднизолон – по 4–8 мг в неделю. Суммарная продолжительность терапии ГКС не должна превышать 12 недель. Поддерживающая терапия иммуносупрессорами проводится не менее 4 лет (УД 1a, СР A).
В отсутствие эффекта от ГКС или при обострении БК после отмены/снижения дозы ГКС (гормонозависимая форма), или неэффективности терапии иммуносупрессорами (рецидив через 3–6 месяцев после отмены ГКС) показана биологическая терапия (инфликсимаб, адалимумаб) или хирургическое лечение (УД 1b, СР A).
 Поддерживающая терапия после достижения ремиссии при помощи биологической терапии проводится инфликсимабом/адалимумабом в комбинации с иммуносупрессорами. Тактика противорецидивной терапии после хирургического лечения описана в разделе 5.5. «Противорецидивная терапия после хирургического лечения БК».
Поддерживающая терапия после достижения ремиссии при помощи биологической терапии проводится инфликсимабом/адалимумабом в комбинации с иммуносупрессорами. Тактика противорецидивной терапии после хирургического лечения описана в разделе 5.5. «Противорецидивная терапия после хирургического лечения БК».
4.6. Тяжелая атака БК (любая локализация)
Тяжелая атака БК требует проведения следующих лечебных мероприятий:
Интенсивная противовоспалительная терапия системными ГКС: преднизолон 2 мг/кг/сут (например, по 25 мг 4 раза в сутки) внутривенно в течение 7–10 дней с последующим переходом на пероральный прием ГКС (преднизолон 1 мг/кг массы тела или метилпреднизолон 8 мг/кг). Первые 5–7 дней целесообразно комбинировать пероральные ГКС с дополнительным внутривенным введением преднизолона по 50 мг/сут.
Назначение иммуносупрессоров: АЗА (2,022,5 мг/кг), 6-МП (1,5 мг/кг), а при непереносимости тиопуринов – метотрексат (25 мг/нед подкожно или внутримышечно).
Антибактериальная терапия (УД5, СР D):
• 1-я линия – метронидазол 1,5 г/сут + фторхинолоны (ципрофлоксацин, офлоксацин) внутривенно 10–14 дней;
• 2-я линия – цефалоспорины внутривенно 7–10 дней.
Данные, полученные при проведении систематических обзоров и мета-анализов, диктуют необходимость дальнейших исследований для оценки целесообразности применения антибиотиков в лечении БК.
Инфузионная терапия: коррекция белково-электролитных нарушений, дезинтоксикация.
Коррекция анемии (гемотрансфузии при уровне гемоглобина < 80 г/л, далее – терапия препаратами железа, предпочтительно парентерально).
Энтеральное питание истощенных пациентов.
По достижении клинической ремиссии дальнейшее лечение (поддерживающая терапия иммуносупрессорами/биологическая терапия, снижение дозы пероральных ГКС) проводится так же, как и при среднетяжелой атаке. В отсутствие эффекта от 7–10-дневной терапии внутривенными ГКС показано проведение биологической терапии (адалимумаб/инфликсимаб) или хирургическое лечение.
4.7. БК с перианальными поражениями
Перианальные проявления при БК часто требуют хирургического лечения, поэтому рассматриваются в разделе 5.5. «Хирургическое лечение перианальной БК».
4.8. БК тонкой кишки (кроме терминального илеита)
При легкой атаке показано назначение месалазина 4 г/сут, прием которого в той же дозе продолжается и в качестве поддерживающей терапии не менее 2 лет (УД 2b, СР B). Следует отдавать предпочтение препаратам с оболочкой (из этилцеллюлозы), обеспечивающей создание достаточной концентрации месалазина в зоне поражения.
Среднетяжелая атака требует проведения системной терапии ГКС в сочетании с иммуносупрессорами: назначается преднизолон 1 мг/кг или метилпреднизолон 0,8 мг/кг (УД 1a, СР A) в комбинации с иммуносупрессорами: АЗА (2,0–2,5 мг/кг), 6-МП (1,5 мг/кг), а при непереносимости тиопуринов – метотрексат (25 мг/нед подкожно или внутримышечно). При наличии инфильтрата брюшной полости назначаются антибиотики: метронидазол внутривенно + фторхинолоны (преимущественно) парентерально 10–14 дней (УД 1a, СР A). При необходимости назначают нутритивную поддержку (энтеральное питание).
По достижении ремиссии поддерживающая терапия проводится иммуносупрессорами в течение не менее 4 лет. Неэффективность терапии ГКС или развитие гормональной зависимости является показанием к назначению биологической терапии: инфликсимаба/адалимумаба.
Лечение тяжелой атаки описано в разделе 4.6, но обязательным дополнением является нутритивная поддержка (энтеральное питание).
4.9. Отдельные аспекты терапии
При проведении гормональной терапии постепенное снижение дозы ГКС до полной отмены является строго обязательным. Суммарная продолжительность гормональной терапии не должна превышать 12 недель. В период применения ГКС показан сопутствующий прием препаратов кальция, витамина D (профилактика остеопороза), ингибиторов протонной помпы, контроль уровня глюкозы крови.

При назначении иммуносупрессоров (АЗА, 6-МП, метотрексат) следует помнить, что их действие, обусловленное терапевтической концентрацией препарата в организме, развивается в среднем в течение 3 месяцев для тиопуринов и 1 месяца для метотрексата.
В период терапии рекомендуется ежемесячный контроль уровня лейкоцитов.
Перед проведением биологической (антицитокиновой) терапии обязательны консультация врача-фтизиатра и скрининг на туберкулез (квантифероновый тест, а при невозможности его проведения – проба Манту, диаскин-тест). Строгое соблюдение доз и графика введения лекарств обязательно. Нерегулярное введение биологических препаратов повышает риск аллергических реакций и неэффективности лечения.
Терапия инфликсимабом проводится в стартовой дозе 5 мг/кг и включает индукционный курс из трех инфузий по схеме 0–2–6, т. е. со вторым введением препарата через 2 недели и третьим – через 6 недель после первой инфузии. В рамках дальнейшей поддерживающей терапии инфузии проводятся каждые 8 недель. Некоторым пациентам может потребоваться увеличение дозы до 10 мг/кг и сокращение срока введения до 6 недель для достижения эффекта.
Индукционный курс адалимумаба включает подкожные введения в дозе 160, а затем 80 мг через 2 недели. Дальнейшие введения (в рамках поддерживающей терапии) выполняются с 4-й недели от начала лечения по 40 мг подкожно каждые 2 недели.
Биологическую (антицитокиновую) терапию для большей эффективности необходимо сочетать с иммуносупрессивной (АЗА) терапией. Проведение хирургического вмешательства на фоне терапии иммуносупрессорами и биологическими препаратами, как правило, не требует изменения противорецидивной терапии.
Важным аспектом лечения БК является профилактика оппортунистических инфекций. К факторам риска их развития относятся:
- прием лекарственных средств: АЗА, внутривенная гормональная терапия (преднизолон 2 мг/кг или перорально более 20 мг в день в течение более 2 недель), биологическая терапия;
- возраст старше 50 лет;
- сопутствующие заболевания: хронические болезни легких, алкоголизм, органические заболевания головного мозга, сахарный диабет.
В соответствии с Европейским консенсусом по профилактике, диагностике и лечению оппортунистических инфекций при ВЗК такие пациенты подлежат обязательной вакцинопрофилактике.
Необходимый минимум вакцинопрофилактики:
- рекомбинантная вакцина против HBV;
- поливалентная инактивированная пневмококковая вакцина;
- трехвалентная инактивированная вакцина против вируса гриппа.
Женщинам до 26 лет в отсутствие вируса на момент скрининга рекомендуется вакцинация от вируса папилломы человека.
5. Хирургическое лечение болезни Крона
Большинство пациентов с БК в течение жизни переносят хотя бы одно оперативное вмешательство на ЖКТ. Невозможность радикального излечения пациентов с БК нередко приводит к повторным резекциям, увеличивая риск синдрома короткой кишки. Современная тактика хирургического лечения БК направлена на выполнение ограниченных резекций, а при возможности – проведение органосохраняющих вмешательств (стриктуропластика, дилатация стриктур).
5.1. Показания к хирургическому лечению БК
Показаниями к оперативному вмешательству при БК служат острые и хронические осложнения, а также неэффективность консервативной терапии и задержка физического развития.
5.1.1. Острые осложнения БК включают кишечное кровотечение, перфорацию кишки и токсическую дилатацию ободочной кишки.
При кишечном кровотечении экстренное хирургическое вмешательство показано при невозможности стабилизировать гемодинамику пациента, несмотря на переливание эритроцитарной массы и проведение интенсивной гемостатической терапии. Кишечное кровотечение констатируют при потере более 100 мл крови в сутки по данным объективных лабораторных методов (сцинтиграфия, определение гемоглобина в каловых массах гемоглобинцианидным методом) или при объеме каловых масс с визуально определяемой примесью крови более 800 мл/сут. В подобных случаях выполняется резекция пораженного участка кишечника (с наложением анастомоза или без такового) с обязательной интраоперационной энтеро- или колоноскопией.
Перфорация тонкой кишки в свободную брюшную полость является достаточно редким осложнением и обычно возникает либо дистальнее, либо проксимальнее участка кишки с наличием стриктуры. При выявлении угрожающих симптомов (перитонеальные симптомы, свободный газ в брюшной полости по данным обзорной R-графии) показано экстренное хирургическое вмешательство, которое в подобной ситуации может быть ограничено резекцией пораженного отдела с формированием анастомоза или стомы. В случае экстренной операции следует избегать формирования первичного анастомоза без протекции при помощи двуствольной илеостомы.
Перфорация толстой кишки при БК встречается крайне редко. Операцией выбора является субтотальная резекция ободочной кишки с формированием илеостомы.
Токсическая дилатация ободочной кишки является редким осложнением БК и представляет собой не связанное с обструкцией расширение кишки до 6,0 см и более с явлениями интоксикации. К факторам риска токсической дилатации относятся гипокалиемия, гипомагниемия, подготовка кишки к колоноскопии при помощи осмотических слабительных и прием антидиарейных препаратов. О развитии токсической дилатации свидетельствует внезапное сокращение частоты стула на фоне имевшейся диареи, вздутие живота, а также внезапное уменьшение или исчезновение болевого синдрома и нарастание симптомов интоксикации (нарастание тахикардии, снижение артериального давления). Операцией выбора является субтотальная резекция ободочной кишки с одноствольной илеостомией.
5.1.2. Хронические осложнения включают стриктуры, инфильтрат брюшной полости, внутренние или наружные кишечные свищи и наличие неоплазии.
5.1.3. Неэффективность консервативной терапии и задержка физического развития
О ней свидетельствует наличие гормональной зависимости и резистентности (см. раздел 2.2 «Классификация БК»). Проявлением неадекватной лекарственной терапии является также задержка физического развития, чаще всего возникающая при поражении верхних отделов ЖКТ.
5.2. Хирургическое лечение БК тонкой кишки и илеоцекальной зоны
Подобную локализацию имеют приблизительно треть всех пациентов с БК, и она часто осложняется формированием стриктуры подвздошной кишки или илеоцекального клапана. Операцией выбора является резекция илеоцекального отдела с формированием илеоасцендоанастомоза.
При выявлении стриктуры после первого курса консервативной терапии (т. е. применения ГКС) в качестве первого этапа лечения показана резекция пораженного участка кишки, а не повторный курс гормональной терапии.
 При наличии активной БК с формированием абсцесса брюшной полости требуется назначение антибиотиков, а также дренирование абсцесса или резекция пораженного участка. Дренирование может осуществляться хирургическим путем или в специализированных центрах и при наличии достаточной квалификации путем чрескожного дренирования. Последний вариант может применяться только в отсутствие стриктуры пораженного участка, что определяет необходимость резекции пораженного отдела.
При наличии активной БК с формированием абсцесса брюшной полости требуется назначение антибиотиков, а также дренирование абсцесса или резекция пораженного участка. Дренирование может осуществляться хирургическим путем или в специализированных центрах и при наличии достаточной квалификации путем чрескожного дренирования. Последний вариант может применяться только в отсутствие стриктуры пораженного участка, что определяет необходимость резекции пораженного отдела.
При наличии непротяженных стриктур тощей или подвздошной кишки, включая стриктуры анастомоза после предшествовавшей резекции, альтернативой резекции является выполнение стриктуропластики, позволяющей избегать обширных резекций тонкой кишки. Выполнение данного вмешательства возможно при длине стриктуры не более 10 см. Противопоказаниями к стриктуропластике служат наличие инфильтрата, абсцесса, злокачественных образований в стенке кишки или активное кровотечение и выраженное воспаление пораженного участка.
В отсутствие инфильтрата и абсцесса предпочтительней выполнение хирургического вмешательства на тонкой кишке и илеоцекальной зоне лапароскопическим способом. Одномоментное формирование двух анастомозов не приводит к увеличению частоты послеоперационных осложнений и частоты рецидива заболевания. Предпочтительной методикой формирования анастомоза на тонкой кишке является наложение аппаратного анастомоза по типу «бок-в-бок», что уменьшает вероятность его несостоятельности и последующего развития стриктуры.
5.3. Хирургическое лечение БК толстой кишки
Ограниченное поражение толстой кишки при БК (менее трети толстой кишки) не требует колэктомии. В этом случае можно ограничиться резекцией пораженного сегмента с формированием кишечного анастомоза в пределах здоровых тканей. При наличии поражения в восходящем отделе ободочной кишки проксимальная граница резекции должна располагаться на уровне средних ободочных сосудов с сохранением последних. Правосторонняя гемиколэктомия показана при выявлении необратимых воспалительных процессов в восходящей и/или поперечной ободочной кишке. В этой ситуации также возможно выполнение расширенной правосторонней гемиколэктомии. При левостороннем поражении выполняется резекция левых отделов с формированием колоректального анастомоза, а при вовлечении в воспалительный процесс также поперечной ободочной кишки возможно формирование асцендоректального анастомоза.
При протяженной БК толстой кишки с тяжелыми клиническими проявлениями операцией выбора является субтотальная резекция ободочной кишки с наложением одноствольной илеостомы. Дистальную часть толстой кишки возможно не резецировать при условии отсутствия в ней выраженного воспаления и вывести на переднюю брюшную стенку в виде одноствольной сигмостомы либо погрузить ушитый конец под тазовую брюшину.
Альтернативной операцией является колпроктэктомия с формированием концевой одноствольной илеостомы. Данное вмешательство выполняется только пациентам с выраженной активностью воспалительного процесса в прямой кишке или тяжелыми перианальными проявлениями, поскольку делает невозможным дальнейшее восстановление анальной дефекации. При этом следует по возможности избегать брюшно-промежностной экстирпации в связи с крайне низкими репарационными возможностями и риском формирования обширных промежностных ран, которые в дальнейшем длительно заживают вторичным натяжением, что инвалидизирует больных и ограничивает их социальную активность.
В отсутствие тяжелых клинических проявлений у пациентов с тотальным поражением толстой кишки при минимальной активности воспалительных изменений в прямой кишке, адекватной функции держания кишечного содержимого и в отсутствие перианальных поражений операцией выбора является колэктомия с формированием илеоректального анастомоза.
Возможность формирования илеоанального резервуарного анастомоза (ИАРА) при БК толстой кишки представляется спорной в связи с высокой частотой осложнений и частым возникновением показаний к удалению резервуара. В то же время средняя продолжительность жизни пациентов после формирования ИАРА без постоянной илеостомы достигает 10 лет, что имеет значение для молодых работоспособных больных. Основные проблемы, угрожающие пациенту с ИАРА на фоне БК, – это развитие перианальных поражений и БК тонкокишечного резервуара.
Операция «отключения» транзита кишечного содержимого по толстой кишке путем формирования двуствольной илеостомы или колостомы показана только крайне истощенным пациентам и беременным женщинам. Данный вид хирургического лечения является временным. Поскольку при ЯК отключение пассажа по толстой кишки не является эффективным, необходимо проведение точной дифференциальной диагностики между БК толстой кишки и ЯК.
Все перечисленные хирургические вмешательства возможно безопасно выполнить с использованием лапароскопических технологий.
При выявлении непротяженной стриктуры толстой кишки возможно выполнение эндоскопической дилатации, однако данная манипуляция связана с более высоким риском рецидива заболевания по сравнению с резекцией пораженного участка кишечника. Выполнение стриктуропластики при стриктурах толстой кишки не рекомендуется.
5.4. Хирургическое лечение БК с поражением верхних отделов ЖКТ
Вовлечение в воспалительный процесс участка кишечника, проксимальнее терминального отдела подвздошной кишки, часто приводит к формированию множественных стриктур и межкишечных свищей, что обусловливает неблагоприятный прогноз БК. В качестве хирургического лечения возможны формирование обходного анастомоза, стриктуропластика и резекция пораженного участка. Прибегать к формированию обходного тонкокишечного анастомоза следует лишь в исключительных случаях из-за высокого риска развития синдрома избыточного бактериального роста в отключенной части тонкой кишки и малигнизации. Обширные резекции способствуют формированию синдрома короткой тонкой кишки. При наличии единичных или множественных непротяженных стриктур операцией выбора может быть стриктуропластика в различных вариантах.
Стриктуры гастродуоденальной зоны (как правило, двенадцатиперстной кишки) поддаются баллонной дилатации. Также эффективным является выполнение стриктуропластики.
5.5. Лечение БК с перианальными поражениями
Перианальные проявления развиваются у 26–54 % больных, страдающих БК, и чаще встречаются при поражении толстой кишки. Наиболее точными методами диагностики являются МРТ малого таза, местный осмотр под обезболиванием и УЗИ ректальным датчиком в условиях специализированного центра. Фистулография обладает меньшей, чем МРТ, точностью при диагностике перианальных свищей.
Целью обследования при перианальных проявлениях БК служит в первую очередь исключение острого гнойного процесса в параректальной области, требующего срочного хирургического лечения.
Подход к хирургическому вмешательству на перианальной области должен быть индивидуальным для каждого пациента.
Перианальные проявления при БК исключают возможность применения салицилатов для поддержания ремиссии и требуют назначения иммуносупрессоров (АЗА, 6-МП, метотрексат) и/или биологических препаратов (инфликсимаб, адалимумаб) в стандартных дозах. Перианальные проявления БК также требуют назначения метронидазола 0,75 г/сут и/или ципрофлоксацина 1 г/сут. Антибиотики применяют длительно (до 6 месяцев или до появления побочных эффектов). Местное применение ГКС и аминосалицилатов при параректальных свищах неэффективно. Целесообразно подключение к терапии препаратов метронидазола в виде свечей и мазей.
При наличии трещин анального канала хирургическое вмешательство не рекомендуется, а отдается предпочтение вышеописанной консервативной терапии.
Простые свищи, не сопровождающиеся какими-либо симптомами, не требуют хирургического вмешательства. Показано динамическое наблюдение на фоне вышеописанной консервативной терапии. При наличии симптомов возможна ликвидация свища при помощи фистулотомии или его адекватное дренирование при помощи установки латексных дренажей-сетонов. Показанием к установке сетонов в большинстве случаев является вовлечение части сфинктера в свищевой ход. В отсутствие воспаления слизистой оболочки прямой кишки возможно выполнение низведения слизисто-мышечного лоскута прямой кишки с пластикой внутреннего свищевого отверстия.
Лечение сложных свищей включает установку латексных дренажей-сетонов в комбинации с агрессивной медикаментозной терапией. С учетом высокой эффективности биологической терапии при надлежащем дренировании сложных свищей оправданно раннее назначение инфликсимаба или адалимумаба. Тем не менее сложные перианальные свищи, с высокой частотой приводящие к развитию гнойных осложнений, часто являются показанием к отключению пассажа по толстой кишке путем формирования двуствольной илеостомы.
Ректовагинальные свищи в большинстве случаев требуют хирургического вмешательства. Лишь в отдельных ситуациях при наличии низкого свища между прямой кишкой и преддверием влагалища возможно проведение только консервативного лечения. В остальных случаях показано оперативное лечение под прикрытием илеостомы. При наличии активного поражения прямой кишки адекватная противовоспалительная терапия до операции увеличивает эффективность вмешательства.
Наиболее неблагоприятным фактором, повышающим вероятность постоянной илеостомы или колостомы, служит наличие стриктуры нижнеампулярного отдела прямой кишки или стеноза анального канала. В большинстве случаев данные осложнения требуют выполнения проктэктомии или брюшно-промежностной экстирпации прямой кишки. В отдельных ситуациях в отсутствие активного воспаления в вышележащих отделах кишечника возможно бужирование стриктуры.
5.5. Противорецидивная терапия после хирургического лечения БК
Даже при полном удалении всех макроскопически измененных отделов кишечника хирургическое вмешательство не приводит к полному исцелению: в течение 5 лет клинически значимый рецидив отмечается среди 28–45 % пациентов, а в течение 10 лет – среди 36–61 %, что диктует необходимость продолжения противорецидивной терапии после операции по поводу БК. К факторам, достоверно повышающим риск послеоперационного рецидива, относятся курение, две и более резекции кишки в анамнезе, протяженные (> 50 см) резекции тонкой кишки в анамнезе, перианальные поражения, пенетрирующий фенотип.
В зависимости от сочетания факторов риска, а также от эффективности ранее проведенной противорецидивной терапии пациенты после операции должны быть стратифицированы на группы с различным риском послеоперационного рецидива. В группе низкого риска рецидива БК целесообразно назначение месалазина (4 г) или сульфасалазина (4 г). Пациенты группы промежуточного риска являются кандидатами на проведение терапии АЗА (2,5 мг/кг/сут) или 6-МП (1,5 мг/кг/сут). Пациентам с высоким риском рецидива целесообразно еще до проведения контрольного эндоскопического исследования начать курс биологической терапии (инфликсимаб, адалимумаб, цертолизумаб пегол).
Противорецидивную терапию рекомендуется начинать через 2 недели после оперативного вмешательства. Спустя 6–12 месяцев всем оперированным пациентам с БК показано проведение контрольного обследования, в первую очередь эндоскопического. При невозможности визуализировать зону анастомоза следует констатировать наличие или отсутствие рецидива, основываясь на сочетании данных рентгенологического обследования (как правило, КТ) и неинвазивных маркеров воспаления – С-реактивного белка, фекального кальпротектина и др.
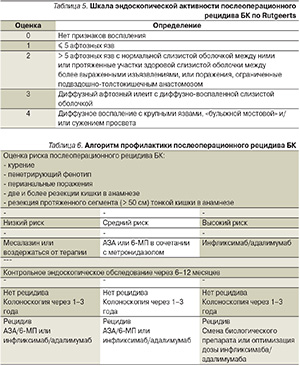
В отсутствие признаков воспаления или при обнаружении минимальных (1 по шкале Rutgeerts) воспалительных изменений (табл. 5) проводимая терапия должна быть продолжена. Наличие более выраженных воспалительных изменений (2–4) указывает на неэффективность проводимой терапии и должно служить показанием к усилению лечения: подключению к иммуносупрессорам пациентов, ранее их не получавших, или проведению биологической терапии адалимумабом или инфликсимабом пациентов, находящихся на поддерживающей терапии (АЗА/6-МП). В дальнейшем вне зависимости от характера течения заболевания и клинической манифестации БК следует не реже раза в 1–3 года выполнять контрольное эндоскопическое исследование, следуя тому же алгоритму выбора противорецидивного средства (табл. 6).
6. ПРОГНОЗ
БК характеризуется прогрессирующим поражением кишечника. На момент установления диагноза осложнения (стриктуры, свищи) обнаруживаются лишь у 10–20 % больных, в то время как в течение 10 лет подобные осложнения развиваются у > 90 % пациентов. В течение 10 лет хирургическое вмешательство в связи с осложнениями и/или неэффективностью консервативной терапии выполняется половине пациентов с БК, а у 35–60 % в течение 10 лет после операции развивается рецидив заболевания. Гормональная зависимость при БК в течение 10 лет хотя бы раз констатируется у 30 % больных.
К прогностически неблагоприятным факторам при БК относятся курение, дебют заболевания в детском возрасте, перианальные поражения, пенетрирующий фенотип заболевания и распространенное поражение тонкой кишки.



