Введение
Остеопороз относится к наиболее распространенным заболеваниям лиц пожилого и старческого возраста.
В России остеопорозом страдают 14 млн человек (10% населения страны), еще у 20 млн граждан России имеется остеопения, которая, как известно, при наличии других факторов риска также может свидетельствовать о высоком риске перелома. Таким образом, в целом 34 млн жителей России имеют высокий риск низкоэнергетических переломов [1]. Значение проблемы остеопороза в первую очередь определяется его последствиями – низкоэнергетическими переломами, обусловливающими значительный рост заболеваемости, инвалидности и смертности пациентов. Каждую минуту в России происходит 7 переломов позвонков, а каждые 5 минут – перелом проксимального отдела бедренной кости (ППОБ) [1]. При этом прогнозы на ближайшие годы в отношении заболеваемости остеопоротическими переломами неутешительны: в связи с увеличением продолжительности жизни общее число основных переломов в России с 2010 по 2035 г. увеличится на 24%, ППОБ – на 41% [2].
Целью лечения остеопороза является снижение риска получения переломов. Это довольно сложная задача, т.к. заболевание имеет многофакторный патогенез, прогрессирующее течение, но в то же время оно характеризуется отсутствием ранних специфических признаков, и полная клиническая картина появляется только при появлении осложнений в виде низкоэнергетических переломов.
Бисфосфонаты в лечении остеопороза
Бисфосфонаты (БФ) стали первым препаратом для лечения остеопороза во всем мире. Этот препарат имеет структурное сходство с гидроксиапатитом кости, благодаря чему они устойчивы к химическому и ферментативному гидролизам в организме. Подобная стабильность молекулы дает возможность значительного увеличения интервалов между повторными введениями лекарственных средств данной группы, и на сегодня мы имеем формы для использования еженедельно, ежемесячно и даже однократно в год, что безусловно способствует повышению эффективности и приверженности пациентов к лечению. В качестве препаратов первой линии БФ включены в современные клинические рекомендации по лечению остеопороза [3].
Механизм действия азотсодержащих БФ основан на подавлении ключевого энзима внутриклеточного мевалонатного пути синтеза холестерина – фарнезилпирофосфатсинтазы. Это приводит к нарушению жизнедеятельности и жизнеспособности остеокластов и обусловливает мощный и длительный антирезорбтивный эффект. Таким образом, основным механизмом действия данных препаратов является снижение скорости костного ремоделирования с угнетением фазы резорбции.
На сегодня БФ относятся к наиболее широко назначаемым препаратам при лечении остеопороза. Данный класс антирезорбентов хорошо изучен в многочисленных клинических рандомизированных плацебо-контролируемых исследованиях. Однако в последние годы отмечены тенденции к снижению частоты инициации терапии пациентами, имеющими высокий риск последующих переломов, и сохранения приверженности к лечению у тех, кто приступил к их приему. Эксперты объясняют это в большинстве случаев преувеличенными опасениями пациентов в отношении риска развития побочных эффектов, в результате чего они отказываются от лечения, которое им жизненно необходимо. Такую проблему в настоящее время называют парадоксом остеопороза [4].
Одним из наиболее известных и имеющих достаточно высокую частоту побочных эффектов при применении БФ является т.н. острофазовая реакция (ОФР), или гриппоподобный синдром. Благодаря ему за БФ закрепилась репутация «тяжелых по переносимости» препаратов. В первую очередь данный побочный эффект свойствен внутривенным БФ редкого введения, особенно золедроновой кислоте. Исследования показали, что среди предикторов неприверженности к длительному использованию данного препарата пациенты с остеопорозом отмечали наличие симптомов ОФР в течение 72 часов после инфузии [5].
В связи с этим изучение особенностей возникновения данного побочного эффекта, а также осведомленность об эффективных мерах, способных приводить к снижению его частоты и/или выраженности, имеют важное значение для клинической практики.
Итак, рассмотрим более подробно механизм развития ОФР. Спустя 48–72 часа после поступления в организм аминобисфосфонатов могут появляться лихорадка, миалгии, артралгии, головные боли, боли в глазах. Большинство из этих реакций слабо или умеренно выражены, симптомы носят транзиторный характер, обычно проходят в течение 3 дней с момента их появления и не требуют лечения. При повторном введении частота встречаемости данного нежелательного явления значительно уменьшается, не превышая 1–2% [6].
В патогенезе развития ОФР лежит блокада аминосодержащими БФ упоминавшегося выше фермента фарнезилпирофосфатсинтазы в остеокластах, что приводит к накоплению предшественников данного пути метаболизма (изопентил пирофосфата и диметилалил дифосфата), которые в свою очередь захватываются моноцитами. Моноциты активируют γδ-T клетки, и они начинают синтезировать провоспалительные (ИЛ-1, ИЛ-6, ФНО-α, ИФН-γ) и пирогенные цитокины [7] (рис. 1). В исследованиях уровень циркулирующего ФНО-α и ИЛ-6 достоверно повышался через 1 и 2 дня после инфузии золедроновой кислоты (р<0,002), а затем снижался до уровней, близких к исходным [7]. Характерными для данного состояния являются также снижение уровня лимфоцитов, эозинофилов и повышение концентрации СРБ в крови.
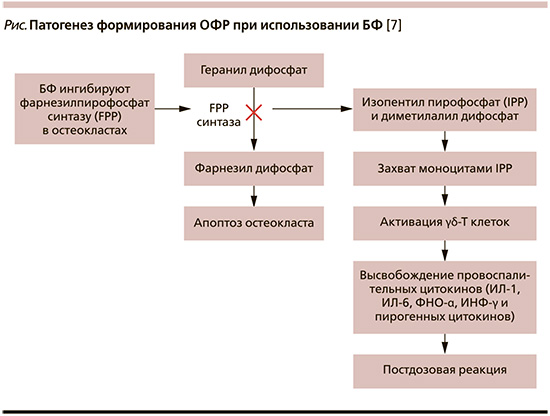
К симптомам ОФР кроме лихорадки относятся также ознобы, мышечно-скелетная боль и артралгии, общая слабость, утомляемость, головная боль, головокружение, тошнота, рвота, судороги. Среди редких реакций описаны единичные случаи увеита, эписклерита, тремора тела во время введения препарата, обморока, припухлости коленного сустава, эритемы лица и аллергической реакции [1, 8].
Оказалось, что данные побочные эффекты являются класс-специфичными для всех аминосодержащих БФ. Наиболее часто они возникают при использовании золедроновой кислоты [9, 10]. Ретроспективный анализ данных исследования Horizon, самого крупного рандомизированного клинического испытания золедроновой кислоты, включившего 7765 женщин с постменопаузальным остеопорозом, выявил, что побочные эффекты в течение 3 дней после введения отмечались в 42,4% случаев при использовании препарата против 11,7% в группе плацебо. Практически в 90% это были реакции легкой или умеренной степени тяжести [9]. Их можно разделить на пять групп симптомов: подъем температуры тела, мышечно-скелетные симптомы (включая боль и припухание суставов), симптомы со стороны желудочно-кишечного тракта (боль в животе, тошнота, рвота), глазные симптомы (воспаление, боль), общие симптомы (включая слабость, назофарингит, отеки).
В исследованиях, проведенных в реальной клинической практике, частота повышения температуры выше 37,5°C после инфузии золедроновой кислоты достигала 63,5%, а всех симптомов ОФР – 75,9% [11].
Есть данные и о частоте этих симптомов после введения ибандроната, она составляет 5–33% [6]. В исследовании P. Sieber et al. [12] проводилась сравнительная оценка частоты ОФР для различных внутривенных БФ, в ходе которого 127 женщин с постменопаузальным остеопорозом получали золедроновую, 145 – ибандроновую кислоту. Общее число пациентов с ОФР было выше в группе золедроновой кислоты (54,3 против 33,1%, p=0,0004). Часть пациентов в обеих группах до введения указанных препаратов использовала в течение определенного времени пероральные БФ. Среди этих пациентов различий в частоте ОФР после инфузии получено не было. Среди бисфосфонат-наивных пациентов ОФР встречалась более часто (68,4%) после золедроновой кислоты по сравнению с инъекцией ибандроната (38,6%), p=0,001.
Даже при пероральном приеме алендроната и ризендроната частота ОФР, зарегистрированная по базе данных FDA, составила 5,6% [13].
Во многих исследованиях отмечено влияние возраста пациентов на частоту развития ОФР. Так, в работе A.D. Аnastasilakis et al. [14] средний возраст пациенток, у которых развились симптомы ОФР, составил 61,7±1,5 года, в то время как больные без реакции были достоверно старше, средний возраст их оказался 67,7±2,1 года, p<0,05. В более крупном исследовании 2017 г. [15], включившем уже 725 женщин, оценивалась переносимость золедроновой и ибандроновой кислот при внутривенном введении. Средний возраст пациенток, имевших хотя бы один симптом ОФР, составил 64,9±9,7 года против 68,6±10,7 у женщин без побочных эффектов, р<0,001.
Для уменьшения симптомов лихорадки, артралгий и миалгий пациентам пробовали назначать нестероидные противовоспалительные препараты (НПВП), например ацетаминофен/парацетамол или ибупрофен. В исследовании J.D. Wark et al. [11] 481 пациентку с постменопаузальным остеопорозом рандомизировали на 4 группы: 1-я группа получала золедроновую кислоту и парацетамол/ацетаминофен 1000 мг каждые 6 часов в течение 3 дней, 2-я группа – золедроновую кислоту и ибупрофен 400 мг каждые 6 часов в течение 3 дней, 3-я группа наряду с золедроновой кислотой использовала по 2 капсулы плацебо каждые 6 часов в течение 3 дней, и 4-я – плацебо внутривенно вместо золедроновой кислоты и капсулы плацебо каждые 6 часов в течение 3 дней. Удивительно, но в группе, получавшей плацебо вместо золедроновой кислоты, в 11% случаев были зарегистрированы симптомы лихорадки и в 17% – другие симптомы ОФР. Следует отметить, что эти данные полностью соответствовали аналогичным показателям в группе плацебо по результатам исследования Horizon [9]. Что это: настроенность пациентов на плохую переносимость и самовнушение, или просто совпадение? Данный результат говорит нам о высокой субъективности в оценке симптомов ОФР, особенно при наличии соответствующих ожиданий больных.
Что касается пациентов в других группах [11], доля женщин с гипертермией и другими симптомами была значительно ниже среди тех, кто получал ибупрофен (соответственно 36,8 и 48,5%) или ацетаминофен/парацетамол (37,3 и 46,3%), в то время как у пациентов без использования НПВП в 64% случаев развивалась лихорадка выше 37,5°C и в 76% – другие симптомы ОФР, p<0,05. Таким образом, данное исследование продемонстрировало, что использование парацетамола и ибупрофена одинаково хорошо уменьшает симптомы после введения золедроновой кислоты.
С той же целью в исследовании E.O. Billington et al. 20 пациентам, ранее не получавшим БФ, во время инфузии золедроновой кислоты была однократно произведена инъекция дексаметазона 4 мг, а другим – плацебо. В результате не было никакой существенной разницы между группами в частоте лихорадки (р=0,95) или других симптомов ОФР (р=0,42) в течение 3 дней после инфузии. Главный вывод, сделанный авторами этого небольшого исследования, в том, что однократная доза дексаметазона 4 мг не влияет на частоту или тяжесть ОФР после первого введения золедроновой кислоты.
Следовательно, премедикация данным препаратом нецелесообразна [16]. Введение глюкокортикоидов в удвоенной или даже утроенной дозе может быть оправданно только в случаях использования золедроновой кислоты для лечения вторичного остеопороза у пациентов с болезнью Аддисона, т.к. при данной патологии описан случай надпочечникового криза у 80-летней женщины с развитием гиповолемии, потребовавшей болюсного введения кортикостероидов [17].
В доклинических исследованиях in vitro доказано, что статины, ингибируя ГМГ-КоА-редуктазу, блокируют бисфосфонат-индуцированную продукцию провоспалительных цитокинов, поэтому было высказано предположение, что их использование поможет избегать развития ОФР. В связи с этим в исследовании Horizon были повторно проанализированы данные о влиянии на переносимость золедроновой кислоты сопутствующего или предшествующего приема статинов. Однако эти данные не нашли подтверждения ни в данном исследовании [9], ни в других исследованиях in vivo для таких препаратов, как аторвастатин, флувастатин, розувастатин [18–20].
В небольшом исследовании китайских ученых был проведен анализ переносимости первой инфузии золедроновой кислоты в группе пациентов, ранее не получавших аминобисфосфонаты (n=78) и получавших эти препараты не менее 1 месяца до инфузии (n=35). Оказалось, что из 35 человек второй группы ни у кого не было зарегистрировано фебрильных цифр лихорадки и только у 2 (5,71%) была субфебрильная лихорадка. В контрольной группе из 78 человек у 33 (42,3%) пациентов было зарегистрировано повышение температуры тела после инфузии золедроновой кислоты. Таким образом, был сделан вывод, что прием аминобисфосфонатов в течение месяца до первой инфузии золедроновой кислоты снижает риск развития лихорадки на 23,1% [21].
В другом исследовании проводилось сравнение частоты ОФР в группах, принимавших в течение 3 месяцев до первой инфузии золедроновой кислоты алендронат, кальцитонин лосося или ралоксифен. В результате также было выяснено, что в первых двух группах достоверно реже фиксировались лихорадка и ОФР [22].
Однако не во всех исследованиях подтверждался подобный эффект предшествующего приема пероральных БФ на частоту и выраженность ОФР. Так, в исследовании на 153 постменопаузальных женщинах с остеопорозом при предшествовавшем инфузии золедроновой кислоты приеме указанных препаратов ОФР развивались реже (33,8 против 52,9% в группе сравнения, р=0,018), но после коррекции по уровню 25(OH)-витамина D такая ассоциация исчезла. Одновременно с этим было отмечено, что у пациенток с ОФР концентрация 25(OH)-витамина D оказалась достоверно ниже по сравнению с женщинами без ОФР (26,3±12,7 против 37,0±13,5 нг/мл, р<0,001). Риск развития данного побочного эффекта был выше у пациентов с уровнем 25(OH)-витамина D <30 нг/мл (OR 4,2; 95% ДИ: 2,1–8,2) [23].
В ретроспективном исследовании китайских ученых для анализа были отобраны 2095 пациентов с остеопорозом, получавших золедроновую кислоту во время госпитализации. Первичной конечной точкой было появление лихорадки выше >37,3°C в течение 3 дней после инфузии. Оказалось, что у пациентов с лихорадкой содержание 25(OH)-витамина D было значительно снижено по сравнению с пациентами без лихорадки, причем повышение его концентрации в сыворотке на 1 нг/мл коррелировало со снижением вероятности лихорадки, вызванной золедроновой кислотой (ОШ=0,86; 95% ДИ: 0,76–0,98, р=0,0188). Авторы сделали вывод, что достижение уровня 25(OH)-витамина D выше 35 нг/мл может быть эффективным способом предотвращения ОФР, вызванных золедроновой кислотой [24].
В исследование F. Bertoldo et al. [25] были включены 90 женщин с остеопорозом, ранее не получавших аминобисфосфонаты. Риск развития ОФР у женщин с дефицитом 25(OH)-витамина D составил: ОШ=5,8, 95% ДИ: 5,30–6,29, p<0,0002, без применения поправок и ОШ=2,38, 95% ДИ: 1,85–2,81, p<0,028, после многочисленных корректировок (по возрасту, индексу массы тела, СРБ, кальцию, паратиреоидному гормону и С-телопептиду коллагена I типа).
Об отрицательной корреляции уровня 25(ОН)-витамина D с частотой и тяжестью ОФР говорят и японские ученые. По их мнению, прием данного витамина снижает также интенсивность мышечно-скелетной боли после введения аминобисфосфонатов [26].
В заключение хотелось бы привести еще некоторые интересные факты [27]. Был проведен дополнительный анализ данных 3-летнего рандомизированного клинического исследования золедроновой кислоты HORIZON-PFT. В анализ были включены 3862 женщины в группу лечения и 3852 женщины в группу плацебо, причем ОФР наблюдалась у 42,4% женщин в группе препарата по сравнению с 11,8% в группе плацебо. Была оценена эффективность терапии женщин с ОФР против тех, у кого эта реакция на фоне введения препарата не была отмечена. Оказалось, что разница в средних изменениях МПК в группе активного лечения по сравнению с плацебо была одинаковой у женщин с ОФР и без нее. Что касается влияния на риск переломов, среди женщин с ОФР риск переломов позвонков был на 51% ниже, чем у женщин без ОФР (OR=0,49, р<0,001). Таким образом, у пациентов, инициирующих терапию золедроновой кислотой, риск переломов позвонков при возникновении ОФР снижается достоверно более значимо, что может быть использовано в клинической практике для повышения приверженности пациентов к лечению.
Заключение
Таким образом, одним из наиболее частых побочных эффектов при использовании группы БФ считается развитие ОФР. Данный побочный эффект является класс-специфическим для этой группы препаратов, особенно часто проявляясь при использовании внутривенных форм. Однако в ходе проведенных исследований показано, что нормализация уровня 25(ОН)-витамина D, использование пероральных БФ до инфузии внутривенных препаратов, а также применение ибупрофена или парацетамола позволяют значительно уменьшать частоту и выраженность данного побочного явления. Сходные результаты относительно предшествующего приема пероральных БФ получены и в проведенном нами ретроспективном исследовании.
В связи с высокой эффективностью класса БФ в качестве препаратов, позволяющих существенно снижать риск любых остеопоротических переломов, а также с учетом терапевтических возможностей влияния на частоту и степень выраженности ОФР необходимо повышать знания врачей и пациентов об этой проблеме. Следует настойчиво добиваться назначения патогенетической терапии пациентам с высоким риском остеопоротических переломов и повышения приверженности к лечению, что остается важным вопросом медицинской этики в лечении остеопороза.



