Введение
Метформин как производное бигуанида (диметилбигуанид) был основным препаратом в гипогликемическом лечении пациентов с сахарным диабетом 2 типа (СД2) с 1950-х гг. С тех пор накоплено множество данных, свидетельствующих о различных эффектах метформина помимо гипогликемического действия. Так, метформин препятствует развитию эндотелиальной дисфункции и окислительного стресса, улучшает гемостаз, благоприятно воздействует на факторы риска (липиды, массу тела, артериальное давление), а также оказывает положительное влияние на защиту сердечно-сосудистой системы [1, 2]. В известном Британском проспективном исследовании UKPDS длительное лечение метформином показало снижение сердечно-сосудистой заболеваемости и смертности при СД2 в большей степени, чем другие сахароснижающие препараты, предполагая, что протективное действие метформина выходит за рамки контроля гликемии [3].
Впервые в мета-анализе 35 крупных долгосрочных рандомизированных клинических исследований (РКИ, n=18 472), изучавших сердечно-сосудистые исходы, установлено преимущество применения метформина по снижению риска сердечно-сосудистых событий (относительный риск [OР]=0,79; p=0,031) и смертности (OР=0,801; p=0,076) по сравнению с плацебо/отсутствием терапии, и особая польза влияния метформина наблюдалась в более длительных исследованиях (≥52 недель) [4].
В одном из последних мета-анализов 40 РКИ (n=1 066 408) также показано значимое снижение риска сердечно-сосудистой и общей смертности, сердечно-сосудистых событий у пациентов с ишемической болезнью сердца (ОР=0,81, ОР=0,67 и ОР=0,83 соответственно; р<0,00001) [5].
Было предложено несколько механизмов кардиопротективного эффекта метформина. Среди них: активация 5’-аденозинмонофосфат-активируемой протеинкиназы (AMPK) и увеличение соотношения AMP:ATP посредством ингибирования митохондриального комплекса 1, увеличение фосфорилирования эндотелиальной синтазы оксида азота в кардиомиоцитах с увеличением продукции оксида азота, активация протеинкиназы C, которая воздействует на митохондриальные АТФ-чувствительные калиевые каналы (K+-АТФ); активация пути NF-kB в сосудистой стенке, который помогает сохранять/генерировать АТФ, предотвращать некроз/апоптоз, уменьшать окислительный стресс, уменьшать воспаление и предотвращать атеросклероз [6–8].
Метформин и фибрилляция предсердий
Фибрилляция предсердий (ФП) является наиболее распространенной аритмией в клинической практике, известна своим прогрессирующим характером и повышенным риском инсульта [9]. Показано, что специфические стрессоры, такие как сердечная недостаточность, СД, артериальная гипертензия, ишемическая болезнь сердца, ожирение или генетическая предрасположенность, вызывают дилатацию предсердий, интерстициальный фиброз и укорочение эффективного рефрактерного периода предсердий. Повышенное давление в предсердиях при сердечной недостаточности приводит к дилатации и фиброзу предсердий, что является структурным субстратом ФП. Было продемонстрировано, что инсулинорезистентность и СД вызывают структурное, электрическое, электромеханическое и вегетативное ремоделирование предсердий, которые впоследствии становятся аритмогенными субстратами ФП [10]. К механизмам, участвующим в развитии фиброза предсердий на клеточном уровне, относятся увеличение уровня трансформирующего фактора роста TGF-β, экспрессия фактора роста соединительной ткани, увеличение продукции супероксида, аномальная активация белков, связанных с гомеостазом кальция, при этом повышенный кальциевый ток L-типа и снижение натриевого тока могут приводить к увеличению продолжительности потенциала действия, увеличению дисперсии предсердного эффективного рефрактерного периода и замедлению проводимости [11]. В результате сочетание фиброза предсердий и задержки проводимости приводит к разъединению возбуждения и сокращения, способствуя развитию ФП.
И наоборот, наличие ФП способствует усугублению сердечной недостаточности из-за нерегулярного наполнения желудочков, потери сокращения предсердий и неблагоприятному структурному ремоделированию левого предсердия, включая миолиз, отложение гликогена, обеспечивая возникновение порочного круга и сохранение ФП [12].
В экспериментальных условиях показано, что метформин предотвращает неблагоприятное структурное и электрическое ремоделирование предсердий путем ослабления миолиза, снижения образования внутриклеточных активных форм кислорода, ослабления воспаления за счет увеличения числа рецепторов, активируемых пролифератором пероксисом (PPARγ) и адипонектина, уменьшения активности фактора NF-kB и количества провоспалительных адипокинов (интерлейкин-6 [ИЛ-6], фактор некроза опухоли-α [ФНО-α] ), что во многом опосредовано активацией 5’-аденозинмонофосфат-активируемой протеинкиназы – основной мишени действия метформина [13]. Подтверждено потенциальное положительное влияние метформина на электрофизиологию предсердий благодаря изменению экспрессии и сохранению функции кальциевых SK-каналов в предсердных миоцитах [14]. В дополнение, на экспериментальных моделях показано, что метформин обладает антифиброзным действием [15].
Влияние метформина на ФП в клинических исследованиях
В одном из первых когортных исследований, выполненном в Тайване, проводилось изучение протективного действия метформина по развитию ФП при долгосрочном наблюдении [16].
В национальной базе данных ретроспективно сформировали когорту из 645 710 пациентов с СД2, среди которых 85 198 человек применяли метформин, а остальные 560 512 составили группу без метформина. Первичный результат определялся по частоте случаев впервые возникшей ФП в течение периода наблюдения. Через 13 лет наблюдения общая частота развития ФП в когорте составила 1,5%, или 287 на 100 тыс. пациенто-лет, частота ФП в группе пользователей метформина была значительно ниже, чем в группе, не применявшей метформин (245 против 293 на 100 тыс. пациенто-лет; p<0,0001). Кривые Каплана–Мейера выживаемости без ФП среди пациентов с СД показали в группе метформина значительно более высокий совокупный показатель отсутствия ФП в течение 13 лет наблюдения, чем в группе без метформина (p<0,001) (рис. 1). После поправки на сопутствующие заболевания и фармакотерапию метформин независимо защищал пациентов с СД от впервые возникшей ФП с отношением рисков 0,81 (p<0,0001).
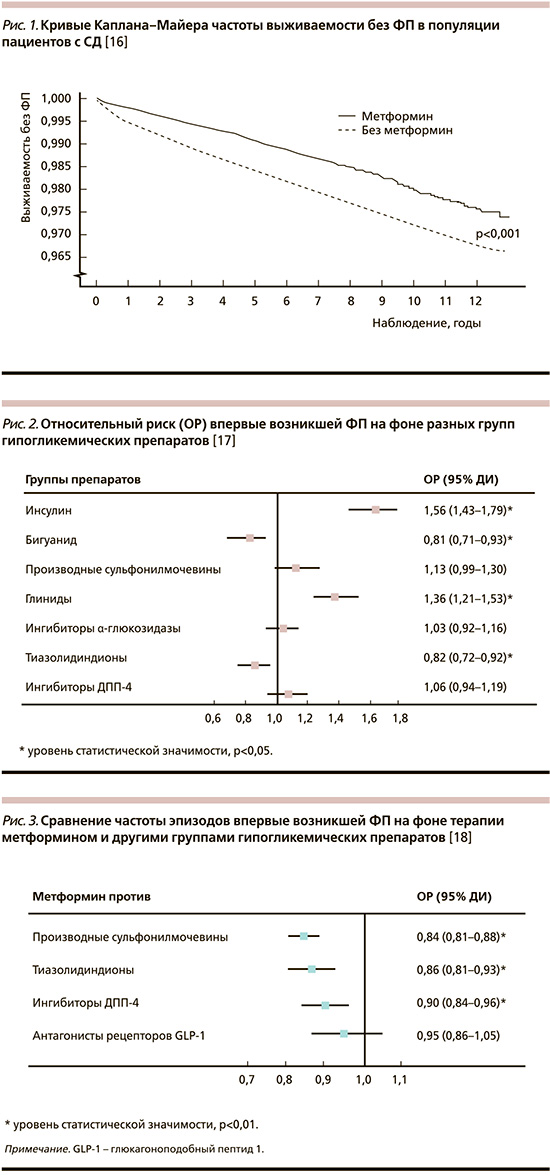
В последующем наблюдательном исследовании «случай–контроль», также выполненном в национальной базе Тайваня, проведено сравнение влияния гипогликемических препаратов разных групп (инсулин, бигуанид, тиазолидиндион, производные сульфонилмочевины, ингибиторы α-глюкозидазы, ингибиторы дипептидилпептидазы – ДПП-4) на популяционном уровне на риск развития ФП [17]. Группу с впервые возникшим эпизодом ФП составили 2882 пациента и 11 428 были отнесены к группе контроля без ФП. Пациенты в группах были сопоставимыми по полу, возрасту, продолжительности СД и индексу коморбидности Чарльсона. В группе пациентов, принимавших бигуанид (метформин) с поправкой на пол, возраст, сопутствующие заболевания и сопутствующее лечение, наблюдался значимо меньший риск развития ФП по сравнению с пациентами, их не принимавшими (ОР=0,81; p<0,05); тогда как в других группах гипогликемических средств существенного влияния не было, а инсулин даже повышал риск ФП (рис. 2).
Недавно получены результаты еще двух когортных исследований, выполненных на популяционных базах данных в США. В крупномасштабном наблюдательном когортном исследовании проведено сравнение частоты развития впервые возникшей ФП на фоне приема метформина (n=190 180) с другими пероральными противодиабетическими препаратами: производные сульфонилмочевины (n=241 917), тиазолидиндионы (n=88 258), ингибиторы ДПП-4 (n=99 050), агонисты рецепторов глюкагоноподобного пептида-1 (n=26 380) [18]. После корректировки влияния факторов риска монотерапия метформином значимо снижала риск развития эпизода впервые возникшей ФП по сравнению с таковой другими группами гипогликемических препаратов (рис. 3).
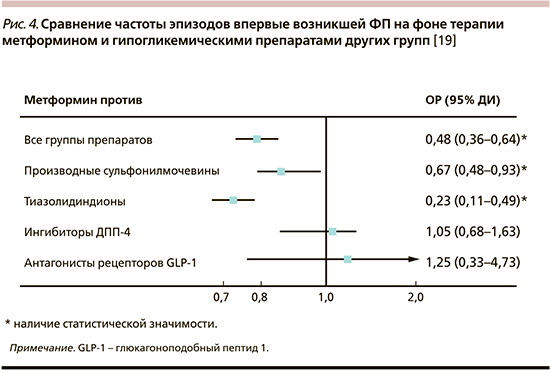
Следующее фармакоэпидемиологическое исследование также направлено на оценку риска развития ФП на фоне терапии метформином и другими гипогликемическими препаратами [19]. Сравнительный анализ проводился в 5 когортах: 1) метформин по сравнению с ингибиторами ДПП-4 (n=1244); 2) метформин по сравнению с тиазолидиндионом (n=288); 3) метформин по сравнению с производными сульфонилмочевины (n=2352); 4) метформин по сравнению с агонистами рецептора GLP-1 (n=258), 5) метформин по сравнению с комбинацией всех четырех групп гипогликемических препаратов (n=3578). Было выявлено, что в группе метформина значимо снижалась вероятность развития ФП (на 52%) по сравнению с объединенной группой гипогликемических препаратов (p<0,001). Использование метформина было достоверно связано со снижением риска ФП по сравнению с препаратами сульфонилмочевины (р=0,018) и тиазолидиндионов (р<0,001), но недостоверно связано с риском ФП по сравнению с агонистами рецепторов GLP-1 и ингибиторами ДПП-4 (рис. 4).
Таким образом, имеются клинические данные, подтверждающие свойство метформина предупреждать развитие ФП. Возможным механизмом такого действия метформина может быть воздействие на эпикардиальную жировую ткань, а также прямое воздействие на миокард, в частности влияние на окислительный стресс [16, 18]. Экспериментальные данные свидетельствуют, что существует связь между окислительным стрессом и ФП: во время тахиаритмии в миокарде предсердий происходит существенное окислительное повреждение и клеточное (ионное и структурное) ремоделирование от активных форм кислорода (АФК), что может индуцировать ФП [16, 18]. Выполненное дополнительное исследование in vitro в культивируемых предсердных миоцитах выявило, что метформин ингибировал индуцированную тахистимуляцией генерацию АФК в предсердных миоцитах и ослаблял деградацию миофибрилл, вызванную тахистимуляцией, снижая степень клеточного ремоделирования [16]. Поскольку окислительный стресс опосредует клеточное ремоделирование, вызванное тахикардией, защита, обеспечиваемая метформином, может быть обусловлена ингибированием воспаления и окисления.
В дополнение к вышеописанным эффектам метформина исследовательская группа J.C. Lal et al. из Института геномной медицины НИИ Лернера Кливлендской клиники (США) провела транскриптомный анализ по определению метформина в качестве кандидата на перепрофилирование препарата для лечения ФП [19]. Исследование in silico включило изучение взаимосвязи «лекарство–заболевание» на основе построения модуля заболевания ФП по транскриптомике ткани левого предсердия пациентов с ФП и сетевого анализа «лекарство–мишень». В результате поиска выявлены 491 экспрессирующий ген в ткани сердца при ФП и 9 потенциальных препаратов-кандидатов, среди которых был метформин. При дальнейших исследованиях метформин показал таргетные свойства с экспрессией ряда генов, ответственных за метаболизм кардиомиоцитов и нацеленных на регуляцию метаболической реакции через AMPK, что было подтверждено с помощью анализа экспрессии генов после лечения на предсердно-подобных кардиомиоцитах, полученных из индуцируемых стволовых клеток человека.
Существующие обоснования для применения метформина с целью предупреждения развития ФП послужили фактором для инициирования в мае 2023 г. нового специально спланированного проспективного РКИ – MAFT (Metformin for Atrial Fibrillarion Trial) [20]. Цель этого многоцентрового открытого рандомизированного плацебо-контролируемого клинического исследования – изучить эффективность использования метформина для лечения ФП в снижении числа неблагоприятных основных сердечно-сосудистых событий и смертности. Планируется 2 группы пациентов с СД и ФП по 385 участников в каждой: группа метформина в дополнение к стандартной стратегии контроля частоты/ритма и антикоагуляции и контрольная группа плацебо, длительность наблюдения – 12 месяцев. Первичной конечной точкой является госпитализация по поводу эпизодической ФП или ФП с быстрым или медленным желудочковым ответом (в случае постоянной ФП). Вторичная конечная точка представляет собой совокупность несмертельных серьезных сердечно-сосудистых нежелательных событий (нефатальный инфаркт миокарда и инсульт, госпитализация по поводу сердечной недостаточности и нестабильной стенокардии) или смерти, не связанной с раком. Ожидаемая дата завершения исследования – апрель 2025 г.
Заключение
В настоящее время рассматривается практика перепрофилирования лекарственных препаратов, предназначенных для лечения одной нозологии, в качестве средства для лечения новых заболеваний или состояний. Такая практика применена в условиях пандемии COVID-19 для перепрофилирования некоторых противомикробных препаратов (хлорохин, гидроксихлорохин и др.). Среди большого арсенала гипогликемических препаратов научный интерес вызвал метформин в связи с переоценкой эффективности данной группы средств по влиянию на отдаленные исходы СД в аспекте сердечно-сосудистых событий и смертности.
В ряду таких систематических обзоров выявлен дополнительный сердечно-сосудистый эффект – предупреждение развития ФП у пациентов, получавших метформин для лечения СД. Данному свойству метформина посвящены фундаментальные экспериментальные работы, а также клинические исследования (в основном ретроспективные), которые позволили подтвердить данный эффект как прямой механизм действия метформина и опосредованные эффекты, приводящие к ремоделированию предсердий и развитию ФП, что было подкреплено транскриптомикой.
На этом этапе первостепенное значение имеют дальнейшие исследования надлежащего качества для выяснения положительного влияния метформина на сердечные аритмии.



