Введение
На сегодняшний день язвенная болезнь (ЯБ) и хронические гастродуо-дениты представляют серьезную проблему клинической медицины в связи с высоким уровнем распространенности, омоложением патологии, рецидивирующим течением, а также возможностью формирования осложнений и нарушением качества жизни больных [1]. Полагают, что язвенная болезнь двенадцатиперстной кишки (ЯБДПК) имеет стадийность в своем развитии, начиная с реализации функциональных расстройств, дальнейшего формирования гастродуоденита и завершая процесс язвенным поражением [2, 3]. Тождественность клинических проявлений, секреторной функции желудка, общность инфекционных агентов, а также аналогичные моторные нарушения гастродуоденальной зоны дали основание рассматривать больных эрозивным гастродуоденитом (ЭГД) как угрожаемых по реализации ЯБ.
В то же время, согласно современным медицинским обзорам, при всей несомненной общности патогенетических механизмов девиация в реализации ЯБДПК или ЭГД во многом продиктована генетически предопределенными особенностями реагирования на этиологические факторы стенкой желудка и двенадцатиперстной кишки (ДПК) [4–6]. В связи с этим нам представляется актуальным исследование роли факторов иммунного реагирования в фокусе ассоциаций полиморфных вариантов отдельных групп генов-кандидатов с развитием ЯБДПК и ЭГД у детей. Среди них наиболее актуальным представляется изучение генов цитокинов, являющихся активными участниками воспалительного процесса и предопределяющих его исход [7, 8]. Резюмируя данные литературы, сведения о влиянии генетических полиморфизмов генов семейства интерлейкина-1β (ИЛ-1β) на реализацию и течение эрозивно-язвенных поражений гастродуоденальной зоны у детей представляется наиболее актуальными [5, 7, 8].
Цель исследования: изучить влияние межгенных взаимосвязей полиморфизмов генов кандидатов С (+3953) Т и С (-511) Т гена ИЛ-1β и VNTR полиморфизма гена ИЛ-1RN в развитии ЭГД и ЯБДПК у детей.
Методы
Для решения поставленной задачи было проведено комплексное обследование 100 пациентов (основная группа) с установленными диагнозами ЯБДПК и хронического ЭГД в возрасте от 3 лет 11 месяцев 29 дней до 17 лет 11 месяцев 29 дней. Дети проходили обследование и лечение на базе ГБУЗ АО «Детская городская клиническая больница № 2» в отделении педиатрии, а далее после реформирования медицинского учреждения в условиях гастроэнтерологического отделения ГБУЗ АО ОДКБ им. Н.Н. Силищевой Астрахани в период с 2014 по 2018 г.
Согласно дизайну исследования, пациенты основной группы были разделены на две подгруппы. Первую составили дети в возрасте от 3 лет 11 месяцев 29 дней до 17 лет 11 месяцев 29 дней (M±m=13,78±0,31 года) с диагнозом «язвенная болезнь двенадцатиперстной кишки» (n=46). В данную подгруппу вошли пациенты как с впервые выявленной ЯБ, так и с рецидивирующим течением ЯБДПК. Вторая подгруппа представлена детьми в возрасте с 3 лет 11 месяцев 29 дней до 17 лет 11 месяцев 29 дней (M±m=10,89±0,49 года) с диагнозом ЭГД (n=54).
Контрольная группа для проведения дополнительного биохимического исследования (определения уровней ИЛ-1β, ИЛ-8 в сыворотке крови) и генетического типирования представлена 100 условно здоровыми детьми, сопоставимыми по возрасту (M±m=11,43±0,34 года) и полу с основной группой.
В каждой группе проводился катамнестический анализ с глубиной поиска 3 года. Все пациенты при поступлении в стационар имели клинику, характерную для стадии обострения и после стационарного лечения выписывались для амбулаторной терапии в стадии неполной ремиссии.
Объем обследования и диагностика ХЭГД и ЯБДПК устанавливали в соответствии с действующими клиническими рекомендациями и сформулированы по Международной классификации болезней (МКБ-10, Женева, 1992 г.).
Генотипирование полиморфных маркеров генов цитокинов ИЛ-1β (С (+3953) Т, С (-511) Т) и VNTR полиморфизма гена ИЛ-1RN с помощью полимеразной цепной реакции (ПЦР) и анализа полиморфизмa длин рeстрикциoнных фрагментов. В качестве биологического материала для исследований служили образцы цельной периферической крови. Выделение геномной ДНК проводили из лейкоцитов венозной крови. Для амплификации использовали программируемый термоциклер Терцик фирмы «ДНК-технология». Продукты амплификации подвергали гидролизу соответствующими эндонуклеазами рестрикции. Ферментативный гидролиз ДНК проводили согласно рекомендациям фирмы-изготовителя. Анализ длин рестрикционных продуктов генов проводили электрофоретическим разделением в 6%-ном полиакриламидном геле, приготовленном на 10-кратном трис-боратном буфере в аппарате для вертикального электрофореза с длиной стекла 20–22 см.
Статистическую обработку результатов исследования проводили общепринятыми методами вариационной статистики. Для анализа сведений о частоте исходов в зависимости от наличия фактора риска в данной работе использован непараметрический метод χ2-критерий Пирсона. В том случае, если число ожидаемого явления было меньше 10 хотя бы в одной ячейке, при анализе четырехпольных таблиц рассчитывали χ2-критерий с поправкой Йетса, а если менее 5 – то критерий Фишера. Для оценки ассоциации генотипов и аллелей изучаемых генов с патологическим фенотипом вычисляли показатель отношения шансов (ОШ).
Результаты
В настоящее время рассматривается не только влияние отделенных биаллельных полиморфизмов генов, но и их взаимодействие с построением двух-, трех- и четырехлокусных моделей.
Для решения поставленной цели были исследованы гаплотип полиморфизмов C (+3953) T, С (-511) Т гена ИЛ-1β, а далее трехфакторное взаимодействие (сочетание полиморфизмов генов ИЛ-1β в коллаборации с генотипами полиморфизма rs223466 (VNTR) гена ИЛ-1RN) как в основной и контрольной группе, так и в подгруппах (табл. 1).

Статистически значимыми оказались как двуфакторное, так и трехфакторное взаимодействия между генотипами в основной группе по сравнению с контрольной. Определена статистическая значимость комбинации генотипов СТ+ТТ полиморфизмов С (-511) Т и C (+3953) T на риск формирования у заболеваний детей основной группы (χ2=5,674; df 1; р=0,048, ОШ=6,029, доверительный интервал [ДИ]: 1,236–29,414), в то время как комбинация генотипов СС+ТТ является проективной или снижающей вероятность формирования эрозивно-язвенных заболеваний верхних отделов желудочно-кишечного тракта у детей (χ2=5,181; df 1; р=0,023, ОШ=0,211, ДИ: 0,017–2,66).
Трехфакторное взаимодействие между генотипами ТТ (C+3953) T, СТ (С-511) Т ИЛ-1β и 1/1 (rs223466 гена ИЛ-1RN) обладает предрасполагающим (χ2=5,701; р=0,017, ОШ=9,647, ДИ: 1,149–81,018), в то время как комбинация генотипов СС+ТТ+1/2 ассоциирована со снижением риска формирования ЯБДПК И ЭГД у детей (χ2=6,664; р=0,010, ОШ=0,121, ДИ: 0,017–0,867, табл. 2). Таким образом, данное трехфакторное взаимодействие генотипов генов ИЛ-1β и ИЛ-1RN обладает регуляторным потенциалом на риск возникновения деструктивно-язвенных поражений гастродуоденальной зоны в детской популяции.
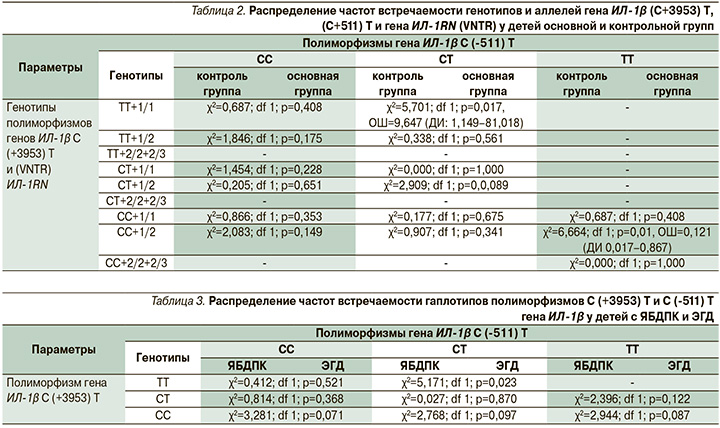
Анализ комбинаций генотипов генов ИЛ-1β+ИЛ-1RN на предрасположенность/устойчивость к ЯБДПК у детей основной группы свидетельствует о статистической значимости трехфакторных и входящих в него двухфакторных взаимодействий представлен в табл. 3, 4.
Комбинированное наследование генотипов СТ+ТТ (полиморфизмов С [-511] Т, С [+3953] Т гена ИЛ-1β) статистически значимо чаще встречалось у больных ЯБДПК, чем у детей с ЭГД (табл. 3). Определено протективное влияние трехфакторного взаимодействия генотипов СС+СС+1/1 (χ2=8,000; df 1; р=0,005, ОШ=0,125) на реализацию ЯБДПК у детей (табл. 4).
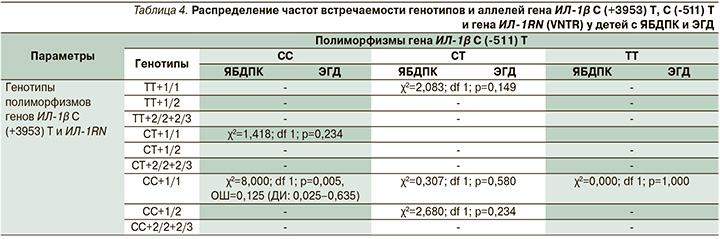
Отсутствие иных ассоциаций в трехфазной модели, по всей видимости, связано с недостаточной численностью когорты обследованных больных (табл. 4).
Обсуждение
Одно из ведущих мест в ансамбле цитокиновой регуляции при ЯБ отводится ИЛ-1β и его антагонисту [9]. Ингибирующая способность ИЛ-1β на кислотность желудка, согласно результатам исследования, проведенного W. Schepp, осуществляется напрямую – через систему комплементарных рецепторов, располагающихся на париетальных клетках [10]. Согласно данным публикаций, ИЛ-1β является не только лидирующим иммунологическим фактором, способным ингибировать выработку соляной кислоты, но и способным запускать каскад про- и противовоспалительных цитокинов [5, 6, 8, 9, 11, 12]. Доказано, что полиморфные варианты гена ИЛ-1β при ЯБ являются высокопродуцирующими. У лиц, гомо- или гетерозиготных по высокородуцирующим аллелям ИЛ-1β усиливается синтез данного цитокина в 2–4 раза, чем у носителей диких аллелей в гомозиготном состоянии [11, 13]. ИЛ-1РА – противовоспалительный цитокин, который, связываясь с рецептором ИЛ-1, препятствует активизации внутриклеточного сигнального каскада этого цитокина [2, 3]. Из множества полиморфных генов цитокинов в развитии воспаления важное значение имеет антагонист рецептора ИЛ-1 (ИЛ-1РА). Согласно проведенным исследованиям, доказано, что у носителей мутантных аллелей, ассоциированных с генетическим перевесом выработки ИЛ-1RA, воспалительный ответ пролонгированный и может приводить к хронизации воспалительного процесса [9, 13]. Известно, что содержание ИЛ-1RA в плазме крови зависит и совместно регулируется генами ИЛ-1β и ИЛ-1RN, а носительство ИЛ-1RN*2 вызывает повышение уровней как циркулирующего ИЛ-1RA, так и ИЛ-1β, активизация последнего является следствием сверхвыработки ИЛ-1RA [7, 8]. Согласно этой версии, при реализации воспалительного ответа у носителей мутантных аллелей происходит избыточное для адекватного воспаления уровня цитокина, что вызывает компенсаторное усиление синтеза ИЛ-1β. В ответ на это вырабатывается еще большее количество ИЛ-1RA. Согласно полученным результатам в ходе исследования, выявленное сочетание гаплотипов и трехфакторных комбинаций генов ИЛ-1β и ИЛ-1RN, определяющих увеличение выработки как ИЛ-1β, так и ИЛ-1RA, может способствовать ульцерогенезу у детей. Можно предположить, что высокие показатели провоспалительных цитокинов выгодны для макроорганизма. Однако при наличии полиморфного варианта ИЛ-1β выработка кислоты ингибируется, Helicobacter pylori колонизирует желудок и воспаление прогрессирует [9, 11].
Таким образом, биалллельные полиморфизмы ИЛ-1β и его рецептора имеют триггерное значение в формировании и реализации ЯБ и ЭГД у детей. Следует отметить, что все значимые комбинации несут генотипы гена ИЛ-1β ассоциированные, по данным литературы, со средним и высоким уровнями продукции ИЛ-1β (генотип ТТ полиморфизма С (+3953) Т и СТ полиморфизма С (-511) Т) и низким или нормальным ответом антогониста ИЛ-1RN (генотипы 1/1, 1/2 ИЛ-1RN). По нашему мнению, ведущее значение в реализации предрасположенности/устойчивости отводится генам ИЛ-1β, однако этот феномен требует дальнейшего изучения.
Выводы
Трехфакторное взаимодействие между генотипами ТТ (+3953), C/T, СТ (С-511) Т), ИЛ-1β и 1/1 (VNTR полиморфизма гена ИЛ-1RN) является предрасполагающим к формированию заболеваний у детей основной группы, в то время как комбинация генотипов СС+ТТ+1/2 ассоциирована со снижением риска реализации ЯБДПК и ЭГД у детей. Гаплотип СТ+ТТ (полиморфизмов С (-511) Т, С (+3953) Т гена ИЛ-1β является предрасполагающим, а трехфакторная модель СС+СС+1/1 – протективной в отношении реализации ЯБДПК у детей. Данные полиморфные варианты обладают регуляторным потенциалом в реализации ЯБДПК.
Вклад авторов. Д.Ф. Сергиенко – концепция и дизайн исследования, написание текста. С.Д. Ихсанов – сбор и обработка материала, редактирование.



