Введение
Гангренозная пиодермия (ГП) (синонимы: молниеносная язвенная пиодермия, язвенно-вегетирующая гангренозная пиодермия, пустулезный язвенный токсико-аллергический дерматит) впервые описана в 1930 г. L. Brunsting, W. Goeckman, О’Leary у пяти пациентов; по другим данным, впервые описана L. Brocq в 1916 г. [1]. Нозологическая сущность заболевания до сих пор вызывает дискуссии. Главную роль в развитии ГП играют особые свойства стафило- и стрептококков [2, 3].
ГП представляет собой тяжелую форму ангиита на фоне сенсибилизации к различным микроорганизмам [4], развивается на фоне выраженных аутоиммунных нарушений (отложение иммуноглобулина М и С3 в эндотелии сосудов, дефекты хемотаксиса, фагоцитоза нейтрофилов и др.), в 5–70% случаев ассоциируется с системными или хроническими воспалительными заболеваниями (язвенный неспецифический колит, болезнь Крона, парапротеинемии, лейкозы) [5].
По мнению В.Д. Елькина и соавт., заболевание не относится к инфекционным или васкулитам, а представляет собой нейтрофильную васкулопатию [2]. J.M. Jackson et al. предполагают неясную этиологию ГП, для которой характерна нейтрофильная инфильтрация дермы с деструкцией ткани [1]. В последние годы ГП выделяют в особую группу воспалительных заболеваний с вовлечением в патологический процесс эозинофилов и нейтрофилов наряду с болезнью Бехчета, синдромом Свита [6, 7].
К основным диагностическим критериям ГП относят возникновение болезненных язвенных дефектов вслед за незначительными травмами (положительный феномен патергии), к дополнительным – частую ассоциацию с такими заболеваниями, как язвенный колит, ревматоидный артрит, болезни крови, болезнь Крона, отсутствие или слабая эффективность от традиционного лечения язв, активная положительная динамика от иммуносупрессивной терапии [8].
Клинические проявления ГП начинаются с образования пустул, содержимое которых может быть стерильным, фурункулоподобных высыпаний или пузыря с прозрачным или геморрагическим содержимым. Элементы распадаются с образованием эксцентрически распространяющихся, резко болезненных язв неправильной или овальной формы с подрытыми краями, неровным легкокровоточащим дном, с валиком и зоной гиперемии по периферии. Отделяемое язв – гнойно-кровянистое с неприятным запахом. Течение ГП хроническое со склонностью к рецидивам и росту зоны поражения.
Терапия ГП представляет значительные трудности. Предлагается применение системных глюкокортикостероидов (сГКС), цитостатиков, биоинженерных препаратов, антибиотиков, вазоактивных препаратов, лазеро- и магнитотерапии, эфферентных методов [9–12].
В доступной литературе мы не встретили описаний сочетания ГП с таким тяжелым аутоиммунным заболеванием, как вульгарная акантолитическая пузырчатка (АП).
Клинический случай
Пациент П. 42 лет впервые заболел в феврале 2016 г., когда появились эрозии в полости рта. До конца мая 2016 г. лечился у стоматологов с диагнозом «cтоматит, лейкоплакия». В связи с неэффективностью лечения был направлен к дерматологу. При цитологическом исследовании обнаружены акантолитические клетки. Выставлен диагноз «акантолитическая вульгарная пузырчатка». Назначено лечение: преднизолон 100 мг/сут, инфузионная терапия, цефтриаксон 1,0 г 2 раза в сутки, препараты калия, кальция. Отмечал улучшение. Однако в августе 2016 г. на фоне приема поддерживающей дозы преднизолона (20 мг/сут) стал отмечать появление язв на бывших эрозированных участках. При повторной консультации дерматолога было рекомендовано увеличение суточной дозы преднизолона до 90 мг/сут, но, несмотря на это, язвы сохранялись, суточная доза была снижена до 50 мг.
В октябре 2016 г. пациент был госпитализирован в дерматологическое отделение Областной клинической больницы № 1 Волгограда. При осмотре в паховых складках и подмышечных впадинах отмечались глубокие язвы овальной и неправильной форм размером от 2 до 5 см с серозно-гнойным отделяемым, по периферии – возвышающийся валик, при пальпации – болезненность.
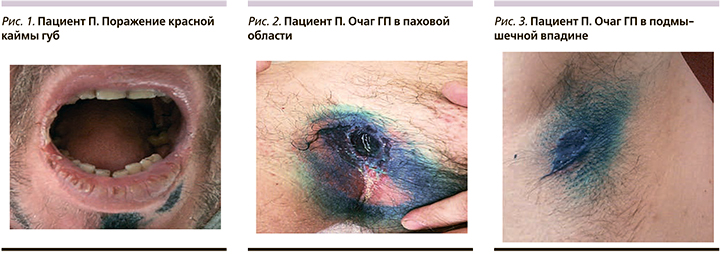
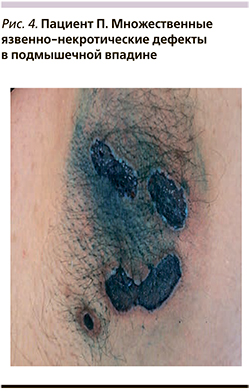 В полости рта и на красной кайме губ имелись эрозии с геморрагическими корками, отдельные – с белесоватым налетом (рис. 1–4). Пациенту назначено лечение: метилпреднизолон 100 мг/сут, азатиоприн по 1 таблетке 3 раза в сутки, затем метотрексат 2,5 мг 2 раза в сутки 5-дневными циклами, пенициллин 1 млн ЕД 5 раз в сутки, Аспаркам, витаминотерапия. На фоне лечения эрозии в полости рта эпителизировались, однако глубокие язвенные дефекты в складках сохранились. Пациент был консультирован хирургом, диагноз – «трофические язвы на фоне АП». Рекомендована обработка язв антисептиками. При посеве отделяемого язв выделена кишечная палочка. С учетом чувствительности назначен азитромицин в дозе 500 мг/сут, однако эффекта от лечения отмечено не было. При повторном посеве имел место рост синегнойной палочки. Консультирован профессором А.Ю. Родиным, выставлен диагноз «гангренозная пиодермия. Акантолитическая вульгарная пузырчатка». Назначен амоксиклав в дозе 1000 мг 2 раза в сутки. По рекомендации клинического фармаколога проведена пульс-терапия Солу-Медролом (метилпреднизолон) 1000 мг/сут, эффекта не было.
В полости рта и на красной кайме губ имелись эрозии с геморрагическими корками, отдельные – с белесоватым налетом (рис. 1–4). Пациенту назначено лечение: метилпреднизолон 100 мг/сут, азатиоприн по 1 таблетке 3 раза в сутки, затем метотрексат 2,5 мг 2 раза в сутки 5-дневными циклами, пенициллин 1 млн ЕД 5 раз в сутки, Аспаркам, витаминотерапия. На фоне лечения эрозии в полости рта эпителизировались, однако глубокие язвенные дефекты в складках сохранились. Пациент был консультирован хирургом, диагноз – «трофические язвы на фоне АП». Рекомендована обработка язв антисептиками. При посеве отделяемого язв выделена кишечная палочка. С учетом чувствительности назначен азитромицин в дозе 500 мг/сут, однако эффекта от лечения отмечено не было. При повторном посеве имел место рост синегнойной палочки. Консультирован профессором А.Ю. Родиным, выставлен диагноз «гангренозная пиодермия. Акантолитическая вульгарная пузырчатка». Назначен амоксиклав в дозе 1000 мг 2 раза в сутки. По рекомендации клинического фармаколога проведена пульс-терапия Солу-Медролом (метилпреднизолон) 1000 мг/сут, эффекта не было.
С учетом неэффективности лечения назначен левофлоксацин 500 мг 2 раза в сутки, цефтазидин 2 г 2 раза в сутки, местно – туалет ран с последующей обработкой химотрипсином. На этом фоне язвы начали активно рубцеваться и через месяц больной был выписан со значительным клиническим улучшением с суточной дозой преднизолона 50 мг/сут.
Обсуждение
По нашему мнению, утверждение С.А. Масюковой и соавт. [13], будто применение сГКС в терапии ГП приводит к быстрому симптоматическому улучшению, спорно, поскольку наш пациент по поводу АП получал мощную противовоспалительную ГКС-терапию (таблетированный преднизолон от 100 мг/сут 1000 мг, Солу-Медрол в виде пульс-терапии без какого-то ни было эффекта). Также сложно согласиться с их утверждением: «…поскольку обсемененение язвы вторично, антибиотикотерапия неэффективна», поскольку именно комбинированная антибиотикотерапия в данном случае показала клиническую эффективность.
Приведенный клинический пример свидетельствует о том, что патогенез ГП сложен, многообразен, возможно, имеет индивидуальные особенности, поэтому заболевание так трудно поддается лечению, особенно на фоне других заболеваний, требующих проведения длительной иммуносупрессивной терапии.
Заключение
Развитие изъязвлений в области эрозий на месте пузырных элементов при АП не служит свидетельством неэффективности лечения пузырчатки и не требует увеличения суточной дозы ГКС, а свидетельствует о присоединении вторичной инфекции на фоне выраженного вторичного иммунодефицита из-за массивной ГКС-терапии.
При развитии ГП на фоне АП рекомендуется назначение двух антибиотиков, потенцирующих друг друга, и местное применение химотрипсина.
Параллельное ГКС-применение цитостатиков и иммунодепрессантов в комплексе с антибактериальной терапией, возможно, позволит снизить риск развития ГП на фоне АП.


