Введение
Пароксизмальная суправентрикулярная тахикардия (СВТ) выявляется более чем у 20% пациентов с нарушением ритма сердца. Этот вид аритмии характеризуется плохой субъективной переносимостью и является предиктором негативного прогноза. Наиболее распространенные причины пароксизмальной СВТ – гипертоническая (ГБ) и ишемическая болезнь сердца (ИБС). Частые и продолжительные пароксизмы СВТ индуцируют аритмогенную дилатацию миокарда и симптомную хроническую сердечную недостаточность (ХСН) [1].
При определенных условиях пароксизмальная СВТ способствует формированию более сложных нарушений ритма сердца. Выраженная суправентрикулярная эктопическая активность ассоциируется с риском развития фибрилляции предсердий, ишемического инсульта и сердечно-сосудистой смерти, даже в отсутствие органических поражений сердца [2, 3]. Пароксизмальная СВТ в ряде случаев сопровождается гемодинамической нестабильностью, что позволяет отнести ее к потенциально жизнеугрожающим сердечным аритмиям.
Для медикаментозной терапии пароксизмальной СВТ наиболее часто используются β-адреноблокаторы (БАБ). Обоснованием их назначения служит блокада симпатоадреналовой системы, часто находящейся в состоянии патологической гиперактивации. Проявляя разносторонние позитивные кардиотропные эффекты, БАБ достоверно снижают риск внезапной сердечной смерти пациентов с органической патологией сердца, замедляют прогрессирование ХСН и уменьшают частоту госпитализаций [4, 5].
Вместе с тем при ряде клинических состояний (брадикардия, атриовентрикулярная блокада, тяжелая систолическая дисфункция левого желудочка [ЛЖ], артериальная гипотензия) применение БАБ лимитировано и сопряжено с риском осложнений. Проаритмические эффекты БАБ являются причиной неблагоприятного исхода для 10–12% пациентов с ИБС [6]. Таким образом, остается актуальной проблема выбора препаратов, избирательно устраняющих аритмию и не ухудшающих функционального состояния организма.
Классические методы оценки функционального состояния, как правило, основываются на изолированном изучении какой-либо вегетативной реакции с помощью электрокардиографии, контроля артериального давления, вариабельности сердечного ритма, функции внешнего дыхания, терморегуляции, кожно-гальванических тестов [7]. Современные требования к контролю результативности медикаментозной терапии подразумевают применение чувствительных диагностических методик, изучающих не только целевые антиаритмические и антиремоделирующие эффекты, но и функциональный резерв целостного организма – толерантность к физической нагрузке, качество жизни, возможность регуляции и адаптации. В литературе нет сведений о контроле влияния БАБ на регуляторно-адаптивный статус (РАС) пациентов с пароксизмальной СВТ. Не исключено, что внутригрупповая гетерогенность БАБ может опосредовать неоднородность влияния различных препаратов на РАС.
Одним из методов оценки РАС является проба сердечно-дыхательного синхронизма (СДС). Аппаратное обеспечение для выполнения исследования относительно недорогое. Проба проста в освоении и не требует длительного обучения специалиста [8]. В последние годы опубликованы результаты достаточного числа клинических испытаний на здоровых лицах и пациентов с различной патологией, где оценка РАС оказалась универсальным, чувствительным и объективным количественным тестом [9–13].
В литературе нет сведений о комплексном определении влияния БАБ на функциональное состояние пациентов с пароксизмальной СВТ с применением метода количественной оценки РАС.
Цель исследования: сравнить клинические эффекты небиволола и соталола на функциональное состояние пациентов с пароксизмальной СВТ.
Методы
В исследование были включены 60 человек с пароксизмальной СВТ на фоне ГБ II–III стадий и/или ИБС. После рандомизации (методом случайной выборки) в группе I (n=30) назначался небиволол, в группе II (n=30) – соталол. Группы были сопоставимыми по возрастным, гендерным и клиническим характеристикам. Начальная доза небиволола составляла 2,5 мг/сут, соталола – 80 мг/сут. Дозы препаратов титровали с интервалом 2–4 недели до 10 и 320 мг/сут соответственно с учетом показателей гемодинамики и индивидуальной переносимости (табл. 1).
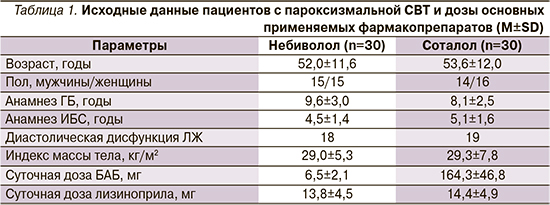
В составе комбинированной терапии все пациенты получали лизиноприл. При наличии показаний назначались аторвастатин в дозе 12,9±4,3 (n=14) и 14,2±4,6 мг/сут (n=15), ацетилсалициловая кислота в дозе 95,8±14,4 (n=16) и 94,8±15,8 мг/сут (n=18) и/или ривароксабан – 20 мг/сут (n=2 и n=2 соответственно).
Критерии включения: пациенты в возрасте от 30 до 70 лет с симптомными неустойчивыми (продолжительностью от 10 до 30 секунд) пароксизмами СВТ по данным СМ ЭКГ на фоне ГБ II–III стадий с сохранной систолической функцией ЛЖ (ФВ ЛЖ≥50%), которые в течение предшествоваших 10 дней не принимали препараты тестируемых групп по не зависящим от исследователя причинам и дали письменное согласие на участие в исследовании после ознакомления с его протоколом.
Критерии исключения: перенесенные острые сосудистые катастрофы, стенокардия напряжения высоких градаций (III–IV функциональных классов), артериальная гипертензия III степени, нарушение систолической функции ЛЖ, наличие противопоказаний к применению тестируемых препаратов, перенесенные кардио- и нейрохирургические вмешательства, наркомания и алкоголизм, декомпенсированная дыхательная, почечная и печеночная недостаточность, злокачественные новообразования, аутоиммунные заболевания в фазе обострения, декомпенсированные эндокринные расстройства, беременность и лактация.
Исследование одобрено Этическим комитетом ГБОУ ВПО «Кубанский государственный медицинский университет» Минздрава РФ (протокол № 34 от 27.02.2001).
Исходно и через 24 недели фармакотерапии выполнялись:
- количественная оценка РАС посредством пробы СДС на программно-аппаратном комплексе ВНС МИКРО (Россия) с определением индекса РАС;
- эхокардиография (Эхо-КГ) в В- и М-режимах с оценкой диастолической функции ЛЖ при импульсноволновой и тканевой допплерографии на ультразвуковом аппарате ALOKA SSD 5500 (Япония) датчиком с частотой колебаний 3,5 МГц для определения структурного и функционального состояния сердца;
- тредмил-тест на аппарате SHILLER CARDIOVIT CS 200 (Швейцария) для выявления скрытой коронарной недостаточности и оценки толерантности к физической нагрузке;
- тест с 6-минутной ходьбой (ТШМХ) для подтверждения или исключения ХСН, определения ее ФК;
- СМ ЭКГ в течение 24 часов на аппарате МИОКАРД ХОЛТЕР (Россия) для выявления пароксизмальной СВТ, контроля эффективности фармакотерапии;
- оценка качества жизни (КЖ) с применением опросника для определения КЖ больного аритмией.
Для статистической обработки полученных данных применены методы вариационной статистики при помощи пакета Statistica (версия 6.0) с расчетом средней арифметической (М), стандартного отклонения средней арифметической (SD) и t-критерия Стьюдента после оценки выборки по критерию Колмогорова–Смирнова. Различия считались достоверными при p<0,05.
Результаты
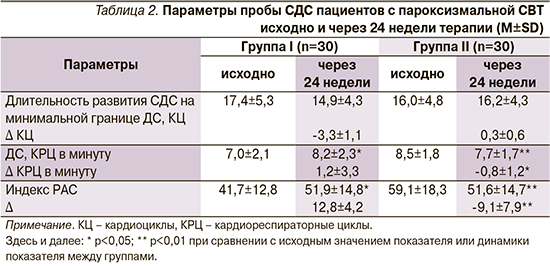
В группе I, по данным пробы СДС, увеличивались диапазон синхронизации ДС на 17,1%; индекс РАС на 24,5%; уменьшилась длительность развития СДС на минимальной границе ДС на 14,4%. Указанные сдвиги демонстрируют повышение РАС.
В группе II уменьшились ДС на 9,4% и индекс РАС на 12,7%; существенно не изменилась длительность развития СДС на минимальной границе ДС. Указанные сдвиги демонстрируют снижение РАС (табл. 2).
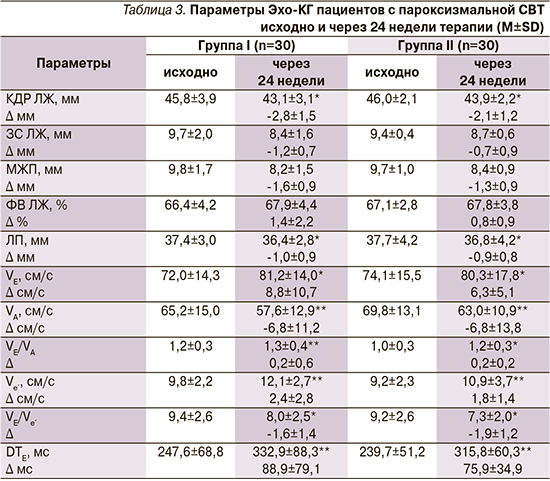
В группе I, по данным Эхо-КГ, увеличились пиковая скорость трансмитрального диастолического потока Е (VЕ) на 12,8%, отношение VЕ и пиковой скорости трансмитрального диастолического потока А–VА (VЕ/VА) на 8,3%, пиковая скорость подъема основания ЛЖ в раннюю диастолу (Ve´) на 23,5%, время замедления трансмитрального диастолического потока Е (DTЕ) на 34,5%; уменьшились конечный диастолический размер (КДР) ЛЖ на 5,9%, передне-задний размер ЛП на 2,7%, отношение VЕ и Ve´ (VЕ/Ve´) на 14,9%, VА на 11,7%; существенно не изменились толщина задней стенки (ЗС) ЛЖ, толщина межжелудочковой перегородки (МЖП) и ФВ ЛЖ. Полученные изменения демонстрируют улучшение структурных и функциональных показателей сердца. В группе II увеличились VЕ (на 8,4%), VЕ/VА (на 20,0%), Ve´ на 18,5%, DTЕ на 31,7%; уменьшились КДР ЛЖ на 4,6%, передне-задний размер левого предсердия (ЛП) на 2,4%, VА (на 9,7%), VЕ/Ve´ на 20,5%; существенно не изменились толщина ЗС ЛЖ, толщина МЖП и ФВ ЛЖ. Указанные сдвиги отражают регресс сердечного ремоделирования, сопоставимый с терапией небивололом (табл. 3).
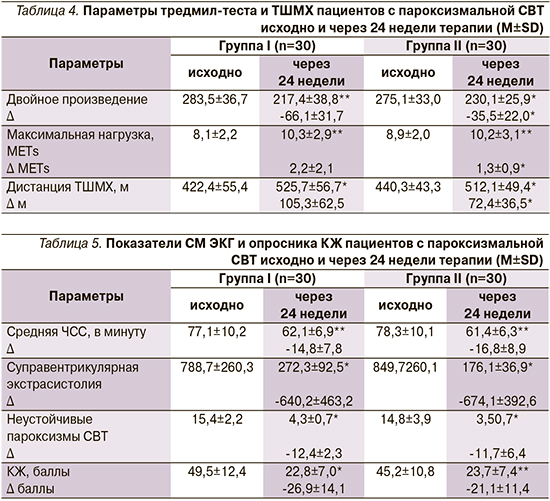
В группе I, по данным тредмил-теста, увеличилась максимальная нагрузка на 27,2%, уменьшилось двойное произведение на 23,3%. В группе II увеличилась максимальная нагрузка на 14,6%, уменьшилось двойное произведение на 16,3%.
В группе I, по данным ТШМХ, увеличилась пройденная дистанция на 24,5%. У 41% пациентов уменьшился ФК ХСН от II до I, в 10% случаев ХСН не регистрировалась. В группе II увеличилась пройденная дистанция на 16,3%; у 30% пациентов снизился ФК ХСН от II до I, в 10% случаев ХСН не регистрировалась. Следовательно, применение небиволола по сравнению с соталолом приводит к более выраженному увеличению толерантности к физической нагрузке (табл. 4).
В группе I, по данным СМ ЭКГ, уменьшились средняя частота сердечных сокращений (ЧСС) на 19,5%, число наджелудочковых экстрасистол на 65,5%, пароксизмов СВТ на 72,1%. В группе II уменьшились средняя ЧСС на 21,5%, число наджелудочковых экстрасистол на 79,3% и пароксизмов СВТ на 76,4%. Полученные результаты свидетельствуют о целевой и сопоставимой антиаритмической эффективности комбинированной фармакотерапии в обеих группах.
В группе I, по данным опросника КЖ пациентов с аритмией, сумма негативных баллов уменьшилась на 53,9%, в группе II – на 47,5%. Следовательно, обе схемы комбинированной фармакотерапии в равной степени улучшают КЖ (табл. 5).
В группе I побочные эффекты возникали в 13% случаев: сухой кашель (1 случай), диспепсия (2), сонливость (1).
В группе II побочные эффекты регистрировались в 17% случаев: сухой кашель (в 2 случаях), диспепсия (в 1), сонливость (в 2). Указанные проявления носили слабовыраженный и преходящий характер, не требовали отмены лечения и исключения из исследования.
Обсуждение
В работе приведена сравнительная многофакторная характеристика результативности применения двух БАБ у пациентов с пароксизмальной СВТ на фоне ГБ II–III стадий и/или ИБС. Небиволол и соталол широко применяются в рутинной кардиологической практике данной группой пациентов. Вместе с тем препараты обладают существенно различающимися фармакохимическими свойствами, чем, вероятно, опосредована неоднородность полученных результатов.
Небиволол – липофильный высокоселективный БАБ третьего поколения, оказывающий вазодилатирующее действие благодаря потенцированию высвобождения оксида азота (NO) из эндотелия сосудов. К дополнительным преимуществам относят позитивное влияние на липидный и углеводный обмены, отсутствие негативного действия на эректильную функцию [14].
Соталол – гидрофильный неселективный БАБ, проявляющий свойства антиаритмических препаратов III класса. Механизм терапевтического действия соталола сопряжен с удлинением фазы реполяризации и потенциала действия кардиомиоцитов, блокадой β1- и β2-адренорецепторов, подавлением функции калиевых каналов. Как все БАБ, соталол уменьшает потребность миокарда в кислороде [15].
В нашем исследовании при лечении соталолом улучшение структурных и функциональных показателей миокарда, целевая антиаритмическая эффективность, повышение толерантности к физической нагрузке сопровождались улучшением КЖ, но снижением РАС. Не исключено, что наряду с достаточным подавлением пароксизмов СВТ препарат действовал угнетающе на симпатический отдел вегетативной нервной системы. В группе пациентов, принимавших небиволол, отмечались сопоставимые органопротективные и антиаритмические эффекты, улучшение КЖ. Однако небиволол положительно влиял на РАС и в большей степени увеличивал толерантность к физической нагрузке.
Поскольку реализация РАС основана на взаимодействии симпатического и парасимпатического отделов вегетативной нервной системы, не исключено, что такие свойства небиволола, как сверхселективность и периферическая вазодилатация, нивелировали его ингибирующие симпатотропные эффекты.
Очевидно, что полученные данные нуждаются в дальнейшем детальном изучении. Не исключено, что применение комплексной оценки результативности терапии, дополненной методом количественной оценки РАС, позволит объективизировать представление о функциональном состоянии, откроет новые перспективы в индивидуализации терапевтической тактики.
Выводы
Обе схемы комбинированной фармакотерапии демонстрировали сопоставимые органопротективные и антиаритмические эффекты, в равной степени улучшали КЖ.
По сравнению с соталолом небиволол отличался позитивным воздействием на РАС и в большей степени увеличивал толерантность к физической нагрузке.
Так как небиволол в большей степени улучшает функциональное состояние пациентов с пароксизмальной СВТ на фоне ГБ II–III стадий и/или ИБС, его применение может быть предпочтительней по сравнению с соталолом.


