Введение
Постакне – это комплекс стойких вторичных изменений кожи, возникающих при длительно существующих воспалительных процессах в элементах акне, порой сохраняющихся даже после их разрешения, и в окружающей интактной коже, а также после применения различных методов инвазивной коррекции [1, 2].
Многокомпонентный патогенез развития поствоспалительной эритемы, нарушений пигментации кожи и рубцовых деформаций диктует необходимость поиска комплексных лечебных методик как в качестве превентивного назначения, так и для коррекции уже сформированных эстетических несовершенств.
Несмотря на различные клинические проявления симптомокомплекса постакне, можно предположить, что в процессы их формирования могут быть вовлечены общие патогенетические механизмы. Получены данные, которые показывают тесное взаимодействие меланоцитов с фибробластами, участвующими в совместной регуляции репарации кожных покровов [3, 4]. В основе патофизиологических реакций на длительно персистирующее воспаление в коже при акне лежит дисбаланс между про- и противовоспалительными цитокинами, матриксными протеиназами и их тканевыми ингибиторами (MMPs и TIMPs), а также факторами роста [5].
Доказано, что тип и количество меланина, вырабатываемого меланоцитами, определяются генетически под влиянием гормональных изменений и воспалительных процессов, накопления продуктов гликирования с возрастом и в результате воздействия УФ-излучения [6]. Важными регуляторами меланогенеза являются производные пептида проопиомеланокортина, α-меланоцитостимулирующий и адренокортикотропный гормоны, которые производятся кератиноцитами, меланоцитами, фибробластами и эндотелиальными клетками нейроэндокринной системы кожи. Пептиды, продуцируемые в эпидермисе, вызывают выработку оксида азота в меланоцитах, регулируют высвобождение из них цитокинов, катехоламинов и серотонина [7]. Таким образом, меланин противодействует эффектам повреждения, вызванного активными формами кислорода в апоптозной ткани. Эти реакции опосредованы высоким уровнем протеаз, которые вызывают разрушение внеклеточного матрикса и деградацию факторов роста. Чрезмерное высвобождение активных форм кислорода приводит к окислительному повреждению, дефициту стволовых клеток, препятствующих регенерации кожи и, соответственно, к высокому риску развития сочетанных нежелательных явлений: стойких дисхромий и патологических рубцовых деформаций [8].
Внутренние факторы, влияющие на развитие этих состояний, включают синтез молекул окружающими кератиноцитами, фибробластами, воспалительными, нервными или эндокринными клетками. Также патологические реакции могут быть обусловлены развитием стойких инфекционных осложнений во время репарации кожных покровов. Немаловажной считается функция апоптозного белка p53, способствующего контролю меланогенеза и неоколлагеногенеза через ряд клеточно-опосредованных механизмов [9]. Определена четкая взаимосвязь тяжести клинических проявлений постакне с фототипом кожи: у пациентов с более темным фототипом даже при легком течении акне неизбежно формируются стойкие поствоспалительные гиперпигментации и рубцы, при этом чаще с избыточным синтезом коллагена [10].
В кожу при длительно заживающих высыпных элементах акне не проникают свежие макрофаги, активно синтезирующие коллагеназу, что способствует нарушению накопления коллагена и определяет характер последующего рубцевания [11]. Именно поэтому основой для градации рубцов постакне служит тип реакции тканей на воспаление – недостаточное синтезирование соединительнотканных волокон (атрофические, у 75% пациентов с акне) или избыточное (гипертрофические и келоидные, возникающие в среднем у 25%).
За последнее десятилетие появились многочисленные доказательства патофизиологической роли накопления конечных продуктов гликозилирования (AGE) в процессах регенерации ран и патологического рубцевания, их влияния на механические и физиологические свойства кожи [12]. Процессы экспосомального хроно- и фотостарения кожи включают снижение пролиферативной способности фибробластов, трофики, иннервации и уменьшение количества кровеносных сосудов, нарушения барьерных функций кожи. Также снижается способность клеточной ДНК к восстановлению, развиваются хромосомные аномалии, генетические мутации и окислительный стресс. Предполагается, что физиологические изменения фибробластов с течением времени, в частности, в результате фотостарения могут влиять на пигментирование кожи. Хотя доказательств взаимосвязи внешнего вида и функциональных свойств тканей сформировавшихся рубцов все еще недостаточно, тем не менее все полученные результаты показывают, что с возрастом увеличивается склонность к появлению стойкой эритемы, поствоспалительной гиперпигментации и рубцов [13]. Следовательно, у пациентов с поздним началом акне, количество которых с каждым годом стремительно увеличивается, риск развития значимо выраженных вторичных структурных и пигментных изменений возрастает.
Большая часть дерматологических исследований в настоящее время направлена на изучение влияния как превентивных методов, так и на оценку результатов терапевтического действия косметологических процедур, топических средств и их комбинаций, направленных на коррекцию уже имеющихся патологических изменений кожи при постакне. Таким образом, обзор и научное обоснование эффективных методов коррекции и профилактики развития симтомокомплекса постакне – актуальная задача исследований в области дерматологии, косметологии, физической и реабилитационной медицины.
Цель исследования: провести анализ доказательных исследований высокого методологического качества по применению различных методов коррекции и профилактики симптомокомплекса постакне.
Методы
Исследование включило поиск высококачественных литературных источников в наукометрических базах данных (PubMed, Google Shcolar, Кокрановский центральный регистр контролируемых исследований [CENTRAL Cochrane database]) с 2016 по 2021 г. и их последующий анализ. В качестве ключевых слов использовали термины на русском и английских языках: рубцы (scars), поствоспалительная пигментация (postinflammatory initiated hyperpigmentation), постакне (postacne), терапия (treatment).
Критериями включения априорного набора были доступные полнотекстовые версии МА (мета-анализов) и СО (систематических обзоров) рандомизированных контролируемых исследований (РКИ) и контролируемых клинических испытаний (ККИ) на английском или русском языках.
Результаты
Результаты многочисленных исследований показывают, что для достижения выраженного и стабильного результата необходимо воздействовать на все звенья патогенеза формирования симптомокомплекса постакне.
Сегодня доказанные стратегии коррекции включают применение топических лечебных средств, внутриочаговых инъекционных методик и использование различных лечебных физических факторов [14–16]. Наиболее популярные методики из ныне используемых – это высокоинтенсивные лазерные технологии, однако их применение все еще ограничивается непредсказуемым ответом на терапию, высоким риском повреждения окружающих тканей и отдаленных рецидивов развития стойкой поствоспалительной как гипо- так и гиперпигментации и рубцевания. При этом целесообразно применять наиболее безопасные методики с минимальной повреждающей способностью: гомогенный фототермолиз неодимовым лазером с Q-Switch-модальностью, фракционный фототермолиз углекислотным и эрбиевым лазерами. Долгосрочные результаты лечения зачастую зависят от приверженности пациента лечению и соблюдению фотозащитного и антисептического режимов после процедур, что также может быть ограничением к их проведению [17–19]. Кроме того, существует необходимость назначения аддитивной пред- и постпроцедурной топической коррекции, минимизирующей развитие осложнений, продиктованной частотой присоединения вторичной инфекции и возможной провокацией появления свежих элементов акне при проведении сеансов лазеротерапии. Как правило, применение таких средств легкое и безболезненное, что повышает шансы добиться клинически значимого результата.
Обзор современных топических и инъекционных лекарственных средств профилактики и коррекции симптомокомплекса постакне представлен в таблице.

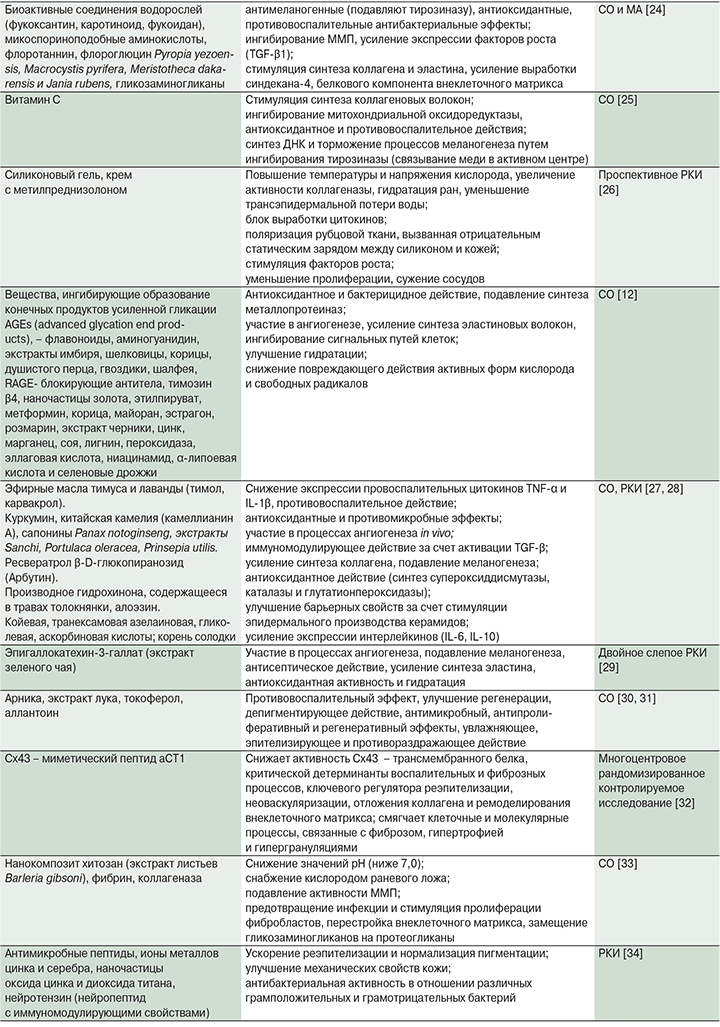
Обсуждение
В последние годы растительные и натуральные депигментирующие и противовоспалительные ингредиенты лечебных средств [12, 27–29] обеспечили альтернативу гидрохинону и глюкокортикостероидам, которые недавно считались «золотым» стандартом в лечении нежелательных пигментаций и кожных рубцовых деформаций, сегодня их применение ограничено в связи с частым развитием побочных явлений: атрофии кожи, телеангиэктазий, пигментных коллоидных милиумов, экзогенного охроноза, пигментации ногтей и катаракты [21, 35].
Изучение вопроса целесообразности назначения местных антибактериальных препаратов с целью профилактики тяжелого течения акне и патологических вторичных изменений показало, что местная доставка антибиотиков из-за высокого риска развития устойчивости и суперинфекции, реакций гиперчувствительности замедленного типа и нарушения регенерации кожных покровов не рекомендуется, если не обнаружена колонизация патогенными штаммами [34].
Широкий спектр биоактивных метаболитов из морских водорослей обладает разнонаправленными воздействиями на кожу, и они могут стать эффективной и рентабельной альтернативой синтетическим продуктам для коррекции нежелательных последствий акне. Однако трудоемкость процессов экстракции, хранения такого космецевтического материала все еще ограничивают возможности широкого их применения. Помимо этого точные механизмы действия этих соединений полностью не изучены.
Одним из популярных и развивающихся направлений клеточных технологий в медицине является разработка методов прямых доставок смеси стволовых клеток (10–30% перицитов, гемопоэтических стволовых клеток), зрелых клеток (фибробластов, эндотелиальных клеток), а также различных цитокинов и факторов роста к месту регенерации кожи [36–39]. Возможно, это позволит контролировать длительность воспалительной фазы, оказывать на нее прямое иммуномодулирующее действие, реконструировать кожу и ее придатки, восстанавливать нормальную пигментацию, иннервацию тканей, т.е. сводить к минимуму риски развития нежелательных поствоспалительных проявлений акне. Однако изготовление подходящих искусственных заполнителей и повязок является очень сложным, трудоемким и дорогостоящим процессом, пока малодоступным широкому кругу пациентов.
Недавние исследования выявили множественную роль арилуглеводородных рецепторов (Aryl hydrocarbon receptors [AhR]) в физиологических процессах в коже. Метаболиты триптофана выделяют среди группы природных и синтетических лигандов AhR. Они включают кинуренин, кинуреновую кислоту и 6-формилиндолокарбазол. Производные триптофана могут регулировать различные сигнальные пути образования симптомокомплекса постакне, поскольку предыдущие исследования подтвердили как минимум частичную роль AhR в патогенезе воспалительных заболеваний кожи и процессах нарушения пигментации [40]. К сожалению, роль самого AhR и биологического влияния его лигандов на профилактику, патогенез и прогрессирование кожных заболеваний до сих пор полностью не изучена.
Еще одной многообещающей субстанцией для таргетной профилактики и коррекции рубцов и других поствоспалительных явлений постакне может стать пропранолол, неспецифический антагонист-β1, -β2 адренергических рецепторов [41]. В нескольких исследованиях показана его противодействующая роль в гиперметаболическом ответе на повышенный уровень катехоламинов при патологическом рубцевании. Механизмы воздействия этого вещества пока не изучены, но, по имеющимся данным, можно предположить, что будущие испытания и внедрение их результатов в практику смогут снизить риск гипертрофического рубцевания.
Заключение
С учетом результатов проведенного анализа литературы можно сделать вывод: перспективными критериями отбора оптимальных методик коррекции и профилактики проявлений симптомокомплекса постакне являются влияние на процессы неоколлагенеза, васкуляризации в тканях, на скорость эпителизации, а также их антисептическая и противовоспалительная активность. При этом можно сделать вывод о необходимости назначения депигментирующих, противовоспалительных и противорубцовых средств как для профилактики на самых ранних сроках формирования симптомокомплекса постакне, так и в качестве терапии уже существующих эстетических недостатков.
С точки зрения современных концепций патогенеза симптомокомплекса постакне целесообразны регулярный поиск, обзор и сравнение эффективности в ходе доказательных исследований новых методов терапии, направленных на профилактику его формирования и коррекцию.
Своевременно начатое терапевтическое воздействие, направленное на правильное формирование новообразованной тканевой структуры, а также уменьшение воспалительной нагрузки, – обязательные составляющие профилактики формирования и коррекции поствоспалительных дисхромий и патологических рубцов кожи при акне.
Вклад авторов. Концепция и дизайн исследования – Н.А. Шанина. Сбор и обработка материала, написание текста – И.Г. Курганская. Редактирование – А.В. Патрушев.


