Введение
Эндоскопическая трансназальная хирургия (ЭТХ) околоносовых пазух (ОНП) в настоящее время стала методом выбора или «золотым» стандартом при различной хирургической патологии в этой области [1].
Основной особенностью ЭТХ ОНП является наличие назального этапа с необходимостью манипулирования в узком протяженном «носовом коридоре». В ряде случаев ЭТХ осуществляется посредством манипулирования несколькими инструментами, что увеличивает травматичность воздействия на слизистую оболочку полости носа.
В связи с наличием назального этапа местные осложнения хирургии ОНП могут вызывать развитие патологических процессов в полости носа. Наиболее известные ринологические осложнения, упоминаемые в литературе, – это синехии, или рубцовая стриктура полости носа, перфорация перегородки носа, рецидивирующие носовые кровотечения, субатрофический ринит, нарушения обоняния, мукоцеле основной пазухи [2]. Для оториноларинголога очевидно отсутствие классификации столь разнообразного числа осложнений, в ряде случаев несущих причинно-следственную связь между собой.
Таким образом, ЭТХ ОНП как любая операция может сопровождаться осложнениями общего характера и, присущими только данному виду вмешательства местными осложнения-ми, для лечения которых применяется большой спектр медикаментозных и немедикаментозных средств, одним из которых является небулайзерная терапия.
Небула́йзер (от лат. nebula – туман, облако) – устройство для проведения ингаляции, использующее сверхмалое дисперсное распыление лекарственного вещества [3]. Впервые термин «небулайзер» был применен в 1874 г. для обозначения «инструмента, превращающего жидкое вещество в аэрозоль для медицинских целей» [4]. Основы научно-практического применения аэрозолей были заложены Л. Дотребандом в 1951 г. [5]. Терапевтический эффект наступает при меньшей дозе вещества и обусловлен тем, что лекарство в форме аэрозоля приобретает огромную суммарную площадь, а следовательно, и более высокую физическую и терапевтическую активность, воздействуя непосредственно на патологический очаг [3, 6].
В зависимости от вида энергии, превращающей жидкость в аэрозоль, различают три основных типа небулайзеров [7, 8]:
- струйные или компрессорные, пневматические, использующие струю газа (воздух или кислород) для генерирования аэрозоля;
- ультразвуковые основаны на образовании аэрозолей под влиянием ультразвуковых колебаний, генерируемых пьезоэлементом;
- Мэшнебулайзеры (мембранные или электронносетчатые), использующие технологию вибрирующего сита (vibrating mesh technology – VMT).
По степени дисперсности выделяют аэрозоли высокодисперсные (размер частиц – 0,05–0,1 мкм), среднедисперсные (размер частиц – 0,1–1 мкм) и низкодисперсные (размер частиц более 1 мкм). Для лечения заболеваний верхних дыхательных путей преимущественно используются аэрозоли средней и низкой дисперсности [9].
Наибольшее применение небулайзерная терапия нашла в пульмонологии при лечении бронхолегочных заболеваний (бронхиальная астма, муковисцидоз, бронхит, ложный круп у детей, бронхоэктатическая болезнь, бронхиолит, альвеолит, легочная гипертензия и др.) [10].
В оториноларингологии небулайзерная терапия применяется в основном в лечении нетяжелых и неосложненных форм острого риносинусита и аденоидита у детей [11, 12], для лечения обострений ларингитов и трахеитов [13] и с целью локальной иммунотерапии в лечении пациентов с вирусассоциированным аллергическим ринитом [14].
К сожалению, несмотря на широкое применение и уникальные терапевтические возможности в отношении терапии верхних дыхательных путей, в доступной литературе отсутствуют данные об использовании небулайзерной терапии пациентов после ЭТХ на ОНП.
Цель работы: оценить эффективность небулайзерной терапии пациентов после ЭТХ ОНП.
Методы
В исследовании участвовал 141 пациент, проходивший лечение в оториноларингологическом отделении Клинического медицинского центра МГМСУ им. А.И. Евдокимова с 2017 по 2020 г. Среди них 90 (63,83%) мужчин и 51 (36,17%) женщина. Возраст пациентов составил от 25 до 66 лет (средний возраст – 49,3±12,5 года).
Распределение пациентов в зависимости от нозологии представлено в табл. 1.
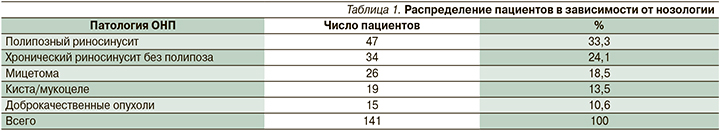
Всем пациентам выполнена ЭТХ ОНП в плановом порядке. Течение операции у всех пациентов характеризовалось отсутствием интраоперационных осложнений. Время операции варьировалось от 45 до 160 минут (среднее время операции – 102,5±36,5 минут), интраоперационная кровопотеря составляла от 250 до 300 мл (средняя кровопотеря – 75±83,3 мл). Проанализировав течение послеоперационного периода исследуемых пациентов, выделены следующие патогенетические «сценарии» исходов ЭТХ ОНП (рис. 1).
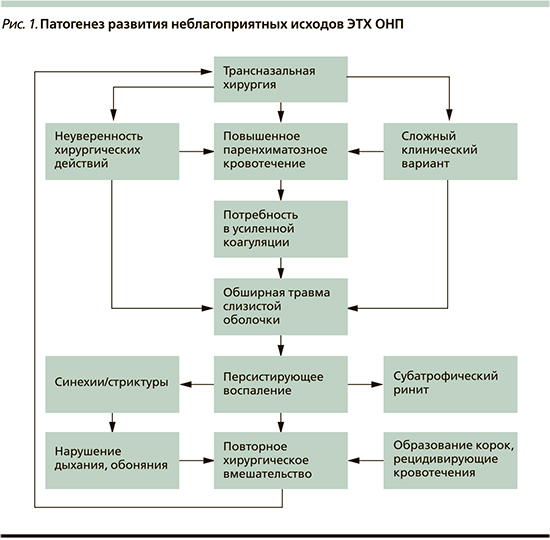
Анализируя представленную схему, можно сделать вывод: все осложнения и последствия отдаленного периода в той или иной степени взаимосвязаны и в какой-то момент может возникнуть «порочный круг» между последствиями хирургии и повторными вмешательствами, которые в этом случае обусловлены не только основным заболеванием со склонностью к рецидивированию (полипозный риносинусит), сколько болезнью оперированных носа и ОНП.
Ведению послеоперационного периода таких пациентов придавали большое значение и анализировали его с точки зрения персонифицированного подхода в зависимости от конкретной нозологии и особенностей клинического статуса. После операции это были стандартные мероприятия, которые начинались в стационаре и продолжались в амбулаторном периоде. Профилактика инфекционного процесса была обязательной с учетом наличия обширной операционной травмы в условиях хронического воспалительного процесса, а также в условиях условно инфицированной раневой поверхности. Обычно назначали интраоперационную антибиотикопрофилактику парентеральными формами цефалоспоринов 4-го поколения, которая продолжалась в послеоперационном периоде (послеоперационная антибиотикотерапия). После выписки пациента из стационара рекомендовали прием пероральных форм антибиотиков той же группы. Общая длительность применения антибиотиков не превышала 7 дней.
Сроки тампонады составляли 1–2 суток и определялись степенью интраоперационной кровопотери и субъективной оценкой врачом состояния системы гемостаза пациентов. Среди тампонов предпочтение отдавали губчатым тампонам, изготовленным из гидролизованного поливинилацетата. После выписки в течение недели рекомендовали домашний режим с исключением физических нагрузок, приема горячих ванн, продуктов с высоким газообразующим потенциалом, форсированного сморкания или натуживания на срок 1 месяц.
Что касается местной медикаментозной терапии, то после удаления тампонов пациент начинал самостоятельные орошения физиологическим раствором через спринцовку или гото-выми формами в виде спреев с морской водой. Туалет полости носа в том виде, в котором он принят в практике оториноларинголога с применением металлических отсосов и другого инструментария, рутинно не производился, поскольку такая тактика сопряжена с дополнительной травмой слизистой оболочки и формирования вторичного инфекционного процесса. Необходимость в его проведении определялась показаниями и обычно отсутствовала, поскольку предложенная схема с орошением каждые 2 часа была эффективной. После выписки пациенты использовали небулайзерную терапию. Поскольку в доступной литературе не найдено схем, в работе была экстраполирована схема ингаляционной терапии острого ларингита после перенесенного эндоларингеального вмешательства, разработанная специалистами ГБУЗ НИКИО им. Л.И. Свержевского ДЗМ [15]:
1. В первые дни после операции применяются ингаляции антибактериальных препаратов: 2 мл 0,01%-ного раствора мирамистина или 2 мл 1%-ного раствора диоксидина в смеси с 3 мл физиологического раствора; флуимицил-антибиотик 1/2 флакона препарата на ингаляцию 2 раза в сутки.
2. Ингаляция дексаметазона 2 мг в 3 мл физиологического раствора 2 раза в сутки 5–7 дней.
3. При повышенном образовании фибриновых пленок к лечению добавляют ингаляции 3 мг химотрипсина или 3 мг трипсина, 5 мг химопсина в 1 мл физиологического раствора, или 0,5%-ного раствора лизоцима по 5 мл 2 раза в сутки затем по 2 мл 3–4 раза в сутки в чистом виде или в разбавлении физиологическим раствором 1:1. Длительность ингаляции – 10 минут.
4. 5,0 мл физиологического раствора или 5,0 мл минеральной воды 4–6 раза в сутки 10 дней или длительно 2 раза в сутки. Длительность ингаляции – 10 минут.
5. При сохранении сухости слизистой оболочки гортани и замедлении процессов эпителизации назначают ингаляции с пеллоидином или гумизолем 2,0 2 раза в сутки. На курс лечения назначают 10 процедур.
С учетом иных нозологических форм в настоящем исследовании схема небулайзерной терапии была модифицирована в зависимости от характера и распространенности патологического процесса. При небольших локальных поражениях ОНП в отсутствие хронического гнойного экссудата она предусматривала ингаляции мирамистином, дексаметазоном и физиологическим раствором в дозировках и кратностью, указанных выше. При распространенном патологическом процессе без сопутствовавшего хронического гнойного воспаления использовали схему диоксидин/дексаметазон/физиологический раствор.
Пациенты с распространенным процессом в условиях эозинофильного или бактериального воспаления или новообразованиями, по поводу которых объем диссекции тканей и широта доступа были существеннее, в послеоперационном периоде требовали усиленной антибактериальной терапии.
В этих наблюдениях назначалась схема флуимуцил антибиотик/дексаметазон/физиологический раствор. Данная комбинация препаратов (антисеп-тик/антибиотик, гормон, физиологический раствор) являлась базовой. Длительность ее применения составляла от 7 при небольших локальных поражениях и до 30 дней при распространенных патологических процессах. В зависимости от потребностей она дополнялась протеолитическими ферментами (химопсин) и биогенными стимуляторами (пеллоидин и гумизоль), которые не применяли при доброкачественных новообразованиях ОНП.
Физиологический раствор как средство для увлажнения слизистой оболочки полости носа применялся в т.ч. самостоятельно несколько раз в день. При невозможности осуществлять небулайзерную терапию более 2 раз в сутки пациентам назначали изотонический раствор морской воды в виде назального душа.
Ведение пациента после трансназальной эндоскопической хирургии ОНП подробно представлено в виде алгоритма на рис. 2.

Такой курс лечения рекомендовался в течение года пациентам с небольшими поражениями. При больших поражениях, не склонных к рецидивированию, курс мог быть пролонгирован до 3 лет, а у пациентов с нозологиями, склонными к рецидивированию (например, полипозный риносинусит), постоянно.
С целью оценки эффективности разработанной методики послеоперационного ведения были сформированы две группы пациентов: основная (ОГ) – 83 (58,87%) пациента, которым проводилась оригинальная методика послеоперационной реабилитации, и группа сравнения (ГС) – 58 (41,3%) пациентов, которым она не проводилась. Группы были однородными по полу, возрасту, основному диагнозу, длительности операции и средней кровопотере (р<0,05).
Оценка эффективности послеоперационной терапии осуществлялась на 14-е сутки, через 1, 4 месяца и через год после операции в зависимости от степени уменьшения объективных и субъективных симптомов заболевания. При этом использовалась визуальная аналоговая шкала (ВАШ), представляющая собой 10-сантиметровую линейку, на одном из концов которой было обозначено «отсутствие симптома», на другом – «максимальная выраженность симптома», 8 промежуточных делений характеризовали плавный переход от одного состояния в другое. Пациент оценивал следующие симптомы: заложенность носа, выделения из носа/стекание по задней стенке глотки, сухость в носу, рецидивирующие кровотечения, головную боль/боль в проекции ОНП, ощущение инородного тела в носу. Врач оценивал состояние слизистой оболочки (сухость, субатрофия, эрозии, бледность, пастозность) и наличие патологического субстрата (отделяемое, корки). Фиксировался средний балл по каждой категории симптомов.
Результаты исследования
Согласно полученным результатам, на 14-е, 30-е сутки лечения выраженность субъективных и объективных симптомов, представленных в баллах, значительно уменьшилась в обеих группах и статистически достоверные различия между средними показателями отсутствовали (p>0,05). Иная ситуация отмечена после прохождения 3-месячного курса назначенной терапии – на 4-й месяц и после окончания наблюдения – 1 год, когда, несмотря на положительную динамику уменьшения клинических симптомов в ГС, в ОГ она была достоверно лучшей (p<0,05) (табл. 2, 3).
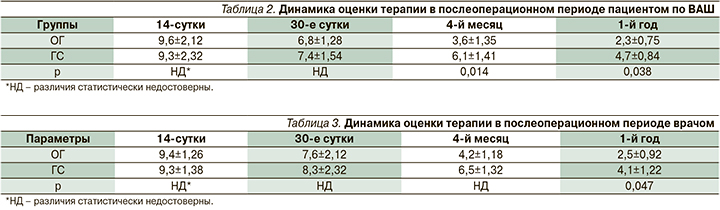
По результатам анализа динамики субъективных и объективных клинических симптомов наблюдалась более быстрая реабилитация в ОГ (р>0,05) по сравнению с ГС, что, вероятно, было связано с соблюдением рекомендованного послеоперационного алгоритма.
Заключение
Проведенное исследование продемонстрировало эффективность предложенной схемы ведения послеоперационного периода у пациентов после ЭТХ ОНП, которая включала интра- и послеоперационную антибиотикотерапию, ирригацию полости носа физиологическим раствором, а также небулайзерную терапию антибиотиками/антисептиками, гормонами и физиологическим раствором. Обоснованность применения вышеуказанной схемы подтверждена значимым уменьшением клинических симптомов в ОГ по сравнению с ГС через 4 месяца после 3-месячного курса терапии. Данная схема лечения характеризуется отсутствием побочных эффектов и позволяет в более короткие сроки достигать реабилитации больных.
Вклад авторов. А.Ю. Овчинников, М.А. Эдже – концепция и дизайн исследования. М.А. Эдже – сбор и обработка материала. М.А. Эдже, Е.В. Марасанова – написание текста. А.Ю. Овчинников, М.А. Эдже – редактирование.


