Введение
Синдром SAPHO (synovitis – синовит, acne – акне, pustulosis – пустулез, hyperostosis – гиперостоз, osteitis – остеит) – хроническое заболевание неизвестной этиологии, к основным проявлениям которого относятся кожный синдром (ладонно-подошвенный пустулез и акне) и патология опорно-двигательного аппарата (остеит и гиперостоз различной локализации и синовиты). Данное заболевание встречается крайне редко, что является основной причиной сложности его изучения и диагностики. Так, согласно ретроспективным исследованиям, среднее время до постановки диагноза составляет 12 месяцев [1].
На текущий момент не совсем ясно место SAPHO-синдрома в классификации ревматологических заболеваний. Так, ввиду частого поражения осевого скелета, формирования энтезитов [2] синдром SAPHO относился к серонегативным спондилоартритам [3], хотя и нетипичного течения, ввиду того что сакроилеит часто имеет односторонний характер [4]. Ряд исследователей предполагают его патофизиологическую близость с аутовоспалительными синдромами, например с хроническим рецидивирующим мультифокальным остеомиелитом (CRMO – chronic recurrent multifocal osteomyelitis) и дефицитом антагониста рецептора интерлейкина-1 ввиду сходной клинической картины (DIRA – deficiency of the interleukin-1 receptor antagonist) [5].
Как отдельная нозологическая форма синдром SAPHO был выделен в 1987 г. A.M. Chamot при описании сходных симптомов у 85 пациентов. За последующие десятилетия в литературе накопились данные о 300 пациентах и их терапии, включая несколько наблюдений в отечественной литературе, что указывает на крайнюю редкость заболевания [6]. С учетом сохранения актуальности тематики SAPHO-синдрома в данной статье нами описано собственное клиническое наблюдение и опыт его лечения.
Клиническое наблюдение
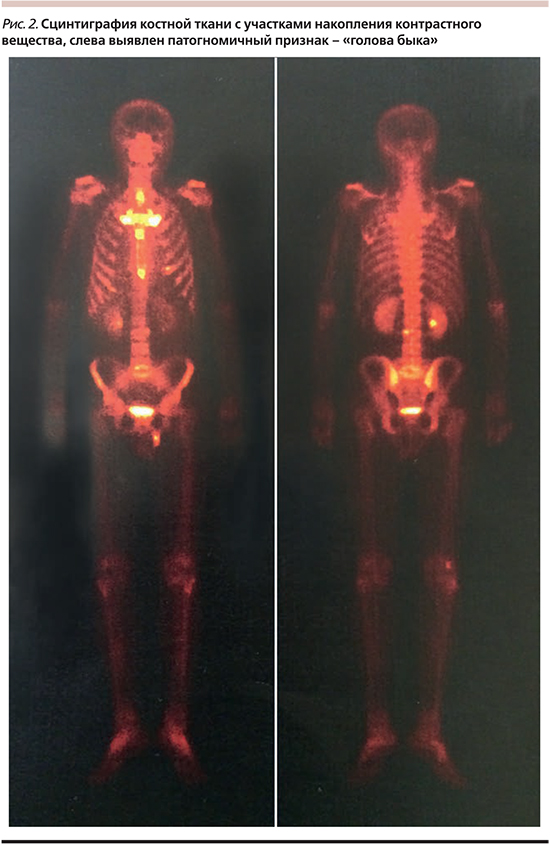
Мужчина 47 лет отметил появление болей воспалительного характера в шейно-грудном отделе позвоночника с мая 2015 г., несколько позже появилась скованность в этом отделе и многоформная сыпь на коже ладоней, с августа – стоп. С данными жалобами пациент обращался к терапевту и дерматологу, получал местную терапию, нестероидные пртивовоспалительные средства (НПВС), проходил курсы физиотерапии, однако не отметив положительной динамики, был направлен к ревматологу. К этому моменту спустя 5 месяцев среди симптомов дополнительно появились боль и скованность в грудной клетке и в поясничном отделе позвоночника, а также боли в проекции левого крестцово-подвздошного сочленения, основными морфологическими элементами сыпи стали пустулы (рис. 1). Объективно при осмотре отмечено уменьшение подвижности в поясничном отделе позвоночника, при пальпации – боли в грудино-ключичных сочленениях. В лабораторных анализах выявлен высокий уровень СОЭ (51 мм/ч), при этом – отрицательные ENA профиль, аССР, аМOV, обследования у инфекциониста и других специалистов. По данным магнитнорезонанс-ной томографии (МРТ) всех отделов позвоночника выявлены участки снижения сигнала в телах позвонков в режиме Т1. Пациент был направлен к ревматологу, в круг дифференциальной диагностики включены аксиальная спондилоартропатия, лимфопролиферативное заболевание. По данным дообследования, включившего МРТ крестцово-подвздошных сочленений, не выявившую признаков сакроилеита, а также отрицательный HLA (Human Leukocyte Antigens)-В27, диагноз спондилоартрита был поставлен под сомнение. В то же время выполнена трепанобиопсия, исключившая лимфопролиферативное заболевание. На основании характерной клинической картины (поражение позвоночника, грудино-ключичных сочленений в сочетании с ладонно-подошвенным пустулезом) заподозрен SAPHO-синдром. По данным сцинтиграфии костной ткани выявлены фокусы накопления препарата, располагавшиеся в зонах деформированных грудино-ключичных сочленений, в грудине (смежных отделах тела и рукоятки, а также тела и мечевидного отростка), что сформировало рентгенологическую картину «головы быка» – патогномоничного признака заболевания (рис. 2). После установления диагноза в связи с отсутствием положительной динамики на фоне терапии НПВС дополнительно назначен курс азитромицина с частичным эффектом: пациент отметил уменьшение болей в шейном и поясничном отделах позвоночника, снижение СОЭ до 23 мм/ч, постепенное заживление пустул. Однако впоследствии после самостоятельной отмены терапии и респираторной вирусной инфекции симптомы возобновились: боли и скованность во всех отделах позвоночника, СОЭ увеличилось до 53 мм/ч, появились пустулы на коже ладоней. Были назначены глюкокортикоиды коротким курсом с последующим переходом на терапию памидронатом 60 мг внутривенно № 3. После первой инфузии отмечена положительная динамика в виде регресса кожного и суставного синдромов, уровень СОЭ уменьшился до 15 мм/ч. Впоследствии ремиссия сохранялась на протяжении трех месяцев, затем пациент вновь отметил незначительные боли в поясничном отделе, появились немногочисленные пустулы на коже ладоней, уровень СОЭ увеличился до 37 мм/ч, в связи с чем был проведен повторный курс инфузий памидроната 60 мг внутривенно № 3 вновь с положительной динамикой, как клинической, так и лабораторной.

На момент описания клинического наблюдения состояние пациента стабильно.
Дифференциальная диагностика
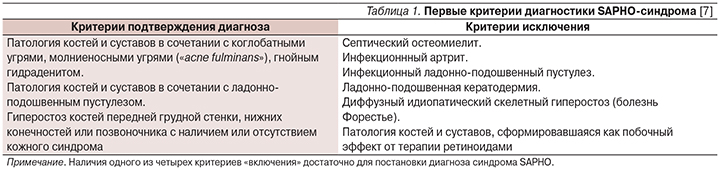
Патология опорно-двигательного аппарата у данного больного достаточно характерна для SAPHO-синдрома: боли в области грудино-ключичных сочленений, боли воспалительного характера в шейном, грудном и поясничных отделах позвоночника. Напротив, кожный синдром имеет неполное проявление, а именно: при наличии ладонно-подошвенного пустулеза отсутствует акне, что можно расценивать как особенность течения заболевания. Тем не менее на основании диагностических критериев, предложенных C.L. Benhamou, диагноз можно считать обоснованным [7] (табл. 1).
При первичном обследовании лабораторно выявлены признаки острой воспалительной реакции в отсутствие специфических лабораторных маркеров, по данным МРТ выявлены признаки изменения костно-мозгового вещества позвонков, в связи с чем в круг дифференциальной диагностики кроме аксиальной спондилоартропатии включено и лимфопролиферативное заболевание, однако результаты дообследования позволили исключить данные нозологии.
Особенности клинической картины и диагностики: данные литературы
Поражение скелета – постоянное, но трудное для дифференциальной диагностики проявление синдрома SAPHO. По данным C. Li и соавт. (2016), среди 164 пациентов у всех наблюдался суставной синдром в отличие от кожного [8]. Начало заболевания, как правило, постепенное: медленно нарастает болевой синдром, появляется скованность. Выявляются повышенные значения СОЭ и С-реактивного белка [9]. У взрослых часто поражаются грудино-ключичные сочленения, кости передней стенки грудной клетки (грудино-реберные сочленения, сочленения рукоятки грудины и тела), в то время как у детей – метафизы трубчатых костей [4]. Остеит при синдроме во многом клинически напоминает бактериальный остеомиелит, но в преобладающем большинстве случаев выделить микроорганизмы из очагов поражения костной ткани не удается. Наряду с деструктивными изменениями в очаге поражения довольно быстро развивается диффузный остеосклероз, а позже за счет неравномерного остеогенеза формируется утолщение кости – гиперостоз [10]. Таким образом, ранние изменения костной ткани деструктивные, а поздние – остеопролиферативные [11]. Гиперостоз в позвоночнике может приводить к сращению позвонков, развитию паравертебральной оссификации, похожей на синдесмофиты или парасиндесмофиты, а в длинных трубчатых костях – на периостит. Патология нижней челюсти формируется в 10% случаев [12].
По данным ранних наблюдений 53 пациентов, поражение кожи формируется в 70% случаев [13]. В более крупных сериях наблюдений выявлено, что у 30% пациентов развитие поражения кожи и скелета происходит одновременно, однако у большей части (60%) пациентов патология кожи формируется чуть позже [2, 14, 15]. Типичным признаком поражения кожи является формирование ладонно-подошвенного пустулеза и тяжелого акне. Наиболее тяжелые формы акне представлены конглобатными или молниеносными угрями («acne fulminans») и гнойным гидраденитом. Важно отметить, что ладонно-подошвенный пустулез не может быть дифференцирован от пустулезного псориаза ни по status localis, ни по гистологии биоптата кожи, что требует дополнительных обследований для исключения поражения скелета в рамках псориатического артрита. Таким образом, диагностика SAPHO-синдрома по изолированному кожному синдрому практически невозможна, в определенных случаях она невозможна и при изолированном суставном синдроме [14, 16].
Отдельно стоит упомянуть, что определенную сложность представляет отсутствие общепринятых критериев диагностики. В 1988 г. C.L. Benhamou были предложены критерии подтверждения и исключения диагноза, которые используются в некоторых работах и до сих пор. Классификационные критерии, разработанные в 2003 г. M.F. Kahn и предложенные на 67-й конференции American College of Rheumaology в октябре 2013 г., широко используются, однако они не могут служить основанием для диагноза (табл. 1, 2).
Лабораторная диагностика SAPHO-синдрома неспецифична, т.е. для него характерны только воспалительные изменения, в то время как визуализционные методики позволяют значительно упростить диагностический путь, а также оценить распространенность процесса. Поражение позвоночника имеет много рентгенологических паттернов, включая признаки неспецифического спондилита, остеосклероза, паравертебральной оссификации, ассиметричного сакроилеита [2, 4, 14]. Компьютерная томография (КТ) позволяет достаточно точно оценить распространенность поражения, включая остеолитические очаги и участки склероза костной ткани, артриты и анкилозы, а сцинтиграфия костей позволяет выявлять латентное поражение за счет изменения метаболизма пораженных участков костного вещества, в связи с чем она служит методикой выбора при клинически неясных случаях [17]. Наиболее специфическим рентгенологическим признаком считают «голову быка», выявляемую при сцинтиграфии костной ткани (рис. 2), формирующуюся за счет энтезопатии грудино-ключичного сочленения и поражения грудины [17]. Сочетанное применение позитронно-эмиссионной томографии с 18-фтордезоксиглюкозой и КТ позволяет исключить неопластические процессы, в т.ч. метастазы костной ткани [18]. МРТ – метод, который наиболее чувствителен к изменениям в мягких тканях, чаще используется при оценке артритов для дифференциальной диагностики, исключения сакроилеитов [19].

Лечение SAPHO-синдрома: данные литературы
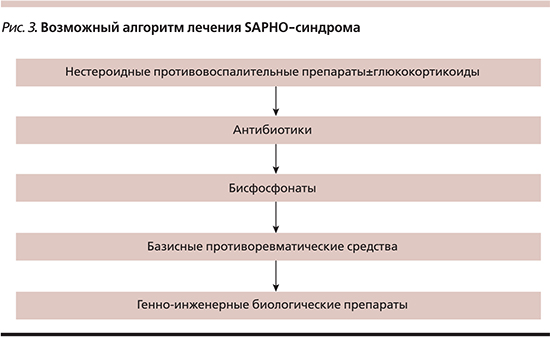
На сегодняшний день рандомизированные контролируемые исследования препаратов, используемых в терапии SAPHO-синдрома, отсутствуют. Выбор режима терапии основывается на опыте применения лекарственного средства в клинических наблюдениях, при этом на основании анализа литературы можно предложить алгоритм терапии (рис. 3). НПВС часто применяются на стадии установления диагноза и служат препаратом выбора в терапии болевого синдрома. Применение глюкокортикоидов системно или интраартикулярно обычно значительно ослабляет костные боли, однако следует отметить, что такой эффект имеет временный характер с последующим обострением как кожного, так и суставного синдромов при попытке снижения дозы препаратов или по завершении их действия [20]. Второй группой потенциально эффективных препаратов можно считать антибиотики, такие как азитромицин, доксициклин [1, 2, 21], в связи с тем что обсуждается патогенетическая роль микроорганизмов как триггерных факторов заболевания. Тем не менее случаи неэффективности терапии, а также рецидивов заболевания достаточно часты, особенно при отмене препаратов. Применение базисных противоревматических препаратов, таких как сульфасалазин, метотрексат, циклопорин, лефлуномид колхицин, было описано в рамках клинических наблюдений со спорными результатами [1, 2, 8, 14].
Обнадеживающие результаты для купирования суставного синдрома наблюдались при использовании бисфосфонатов [1, 22]. Так, в исследовании F. Aljuhani и соавт. (2015) среди 22 пациентов, получавших памидронат, через 6 месяцев у 18 пациентов наблюдался положительный эффект, оцененный врачом, при этом субъективно боли уменьшились на 50% у 17 пациентов и на 100% – у 7 пациентов из 22. Сходные результаты получены в исследовании E. Delаttre и соавт. (2014) от 22 пациентов. Среди побочных эффектов отмечены гриппоподобные реакции, гиперкальциемия, которые, однако, не повлияли на завершение курса [22]. В литературе также описаны случаи успешного применения алендроновой [23], ибандроновой [24], золедроновой кислот [25]. В одном клиническом наблюдении эффективным оказалось сочетание ретиноидов и бисфосфонатов как на кожный, так и на суставной синдром [26].
Использование генноинженерных препаратов также описано при SAPHO-синдроме, при этом наиболее часто применяются ингибиторы фактора некроза опухоли α (иФНО-α), преимущественно инфликсимаб в дозе 5 мг/кг по стандартной схеме [27, 28]. В исследовании F. Aljuhani и соавт. (2014) инфликсимаб получал 1 пациент, при этом отмечен быстрый положительный эффект с сохранением ремиссии в течение 3 лет. Стоит отметить, что, несмотря на положительные результаты со стороны суставного синдрома, рецидивы заболевания проявлялись кожным синдромом. Другими иФНО-α, применяемыми при SAPHO-синдроме, были этанерцепт, адалимумаб и голимумаб [29–32].
В ряде работ была показана эффективность анакинры (антагониста интерлейкина-1), используемой как в качестве препарата первой линии, так и после неэффективного использования иФНО-α [33, 35]. Устекинумаб и секукинумаб (блокатор интерлейкина-12/23 и интерлейкина-17 соответственно) были эффективными в отношение поражения кожи [34].
Заключение
Таким образом, несмотря на редкость, SAPHO-синдром должен включаться в круг дифференциальной диагностики пациентов с наличием воспалительных болей в спине, патологии грудино-ключичных сочленений, а также при характерном кожном синдроме. Сложность постановки диагноза заключается в том, что характерные симптомы могут не сочетаться между собой во времени или иметь не совсем типичное течение, в связи с чем требуется применение более высокотехнологичных методов исследования, таких как сцинтиграфия костной ткани.
На текущий момент существует много препаратов для контроля данного заболевания, что, однако, связано с эмпирическим подходом к его терапии.
С учетом того что инфекция рассматривается как потенциальный триггерный фактор для последующего формирования воспаления, в качестве терапии первой линии следует рассматривать НПВС и антибактериальные препараты (азитромицин, доксициклин). При рефрактерном течении болезни в качестве терапии второй линии возможно использование бисфосфонатов. Несмотря на обнадеживающие результаты применения генно-инженерных биологических препаратов (в основном иФНО-α), данный класс препаратов следует применять в случаях рефрактерного течения болезни.


