Кашель – одна из самых частых причин обращения к врачу в амбулаторной практике. При этом он может быть симптомом большого количества различных заболеваний органов дыхания, сердечно-сосудистой системы, желудочно-кишечного тракта. Нередко симптом «кашель» выходит на первый план и бывает настолько тяжелым, мучительным, что «затмевает» картину основного заболевания, ставшего его первопричиной. И в каждом отдельном случае необходимо принимать решение о лечении пациента. Желание вылечить кашель как можно быстрее и радикальнее часто способствует ошибочным назначениям, приводя к обратным результатам – затягиванию течения острого кашля и переходу его в подострый или хронический [1].
Прежде чем принимать решение о способе лечения кашля, необходимо диагностировать заболевание, одним из симптомов которого является кашель (табл. 1) [2].
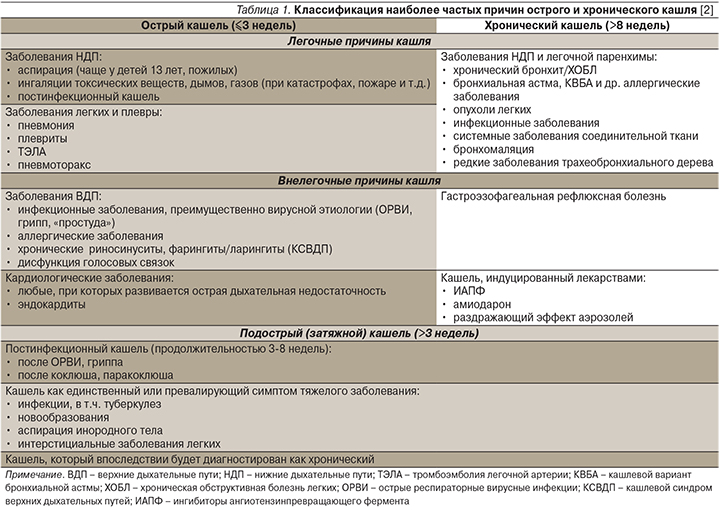
В ряде случаев кашель уступает лечению основного заболевания (этиотропному и/или патогенетическому), например применению ингаляционных глюкокортикостероидов при КВБА, ингибиторов протонной помпы при гастроэзофагеальной рефлюксной болезни (ГЭРБ). Тем не менее существует достаточное количество заболеваний и состояний, при которых возникает необходимость симптоматической терапии кашля (ОРВИ, коклюш, пневмония, состояние после оперативных вмешательств на органах брюшной полости и др.).
Для выбора тактики и стратегии симптоматического лечения кашля необходимо знать его продолжительность (острый, подострый или хронический), иметь представление о наличии или отсутствии мокроты (продуктивный/непродуктивный кашель; табл. 2) [3], ее характере, затруднениях экспекторации и т.д.
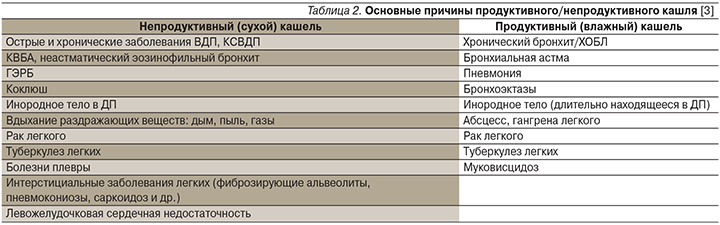
Для патологии НДП характерно развитие продуктивного (влажного) кашля с экспекторацией мокроты. В результате воспалительного/инфекционного заболевания происходит гиперпродукция вязкого бронхиального секрета (БС), как правило сопровождающаяся нарушениями мукоцилиарного клиренса (МЦК) и впоследствие этого – мукостазом. Итак, продуктивный кашель, как правило, сопровождается экспекторацией мокроты – откашливанием избытка вязкой бронхиальной слизи, гноя, продуктов тканевого распада и т.д.
Следует отметить, что эффективность продуктивного кашля (экспекторация мокроты) зависит от многих причин, например фазности течения заболевания. Так, при пневмонии кашель в течение некоторого времени остается сухим, т.к. вследствие высокой вязкости БС он может быть неэффективным. Нарастание обструкции ДП при хроническом бронхите, ХОБЛ, бронхиальной астме может сопровождаться прекращением экспекторации мокроты. Кроме того, в определенных клинических ситуациях (при переломе ребер, других травматических повреждений грудной клетки, после перенесенных хирургических вмешательствах на органах грудной клетки и брюшной полости) больные «противятся» кашлю (табл. 3). [4].
Особенно опасна гиподиагностика неэффективного продуктивного кашля. При неэффективном кашле возможно развитие таких тяжелых осложнений, как пневмония, ателектаз легкого и/или острая дыхательная недостаточность. Гиподиагностика неэффективного продуктивного кашля может способствовать необоснованному назначению противокашлевых препаратов, например, в дебюте пневмонии для подавления сухого неэффективного кашля, изнуряющего больного. Это назначение препятствует осуществлению дренажной функции МЦК, экспекторации БС, удалению патогенных микроорганизмов.

В противоположность этому о непродуктивном кашле мы можем говорить в тех случаях, когда отсутствуют признаки инфекционного воспаления слизистой оболочки НДП, а следовательно, нет и гиперпродукции БС. В качестве классических примеров непродуктивного кашля можно привести ОРВИ у практически здоровых людей, не страдающих хроническими заболеваниями НДП, рак легкого или аллергическое воспаление воздухоносных путей при КВБА (табл. 2). Как правило, непродуктивный кашель связан с раздражением рецепторов кашлевого рефлекса и чаще всего бывает мучительным, надсадным, не приносящим облегчения. Непродуктивный кашель по определению сухой, т.к. не происходит гиперпродукции БС. Поэтому жалобы на сухой кашель свидетельствуют о его непродуктивном характере. В то же время может наблюдаться и ложная продуктивность, например, при постназальном затеке у пациентов с ринитами и/или риносинуситами откашливается назальная слизь.
Установив продуктивность/непродуктивность кашля мы подходим к выбору его симптоматической терапии. Таким образом, симптоматическая терапия кашля может быть направлена либо на облегчение экспекторации мокроты (прокашлевая терапия) либо на его подавление (противокашлевая).
Прокашлевая терапия
В настоящее время существует большое количество лекарственных средств, так или иначе влияющих на реологию БС и МЦК [5]. По основному механизму действия на БС их можно разделить на 4 группы – экспекторанты, муколитики, мукокинетики и мукорегуляторы. (табл. 4) [6]. Деление это в большой степени условно, т.к. и представители группы мукокинетиков (амброксол), и представители группы мукорегуляторов (карбоцистеин) способны расщеплять межмолекулярные связи мукополисахаридов БС, хотя и в меньшей степени, чем муколитики (N-ацетилцистеин – NAC). В конечном итоге все мукоактивные препараты рано или поздно, облегчая экспекторацию БС, уменьшают и/или прекращают кашель. В то же время особенности механизмов действия, времени наступления эффекта наиболее часто и успешно применяемых мукоактивных средств (фитопрепараты, бромгексин, амброксол, NAC и карбоцистеин) требуют внимания врачей к правильному подбору препарата в каждом конкретном случае [7]. В этой статье мы остановимся на наиболее часто используемых мукоактивных препаратах.
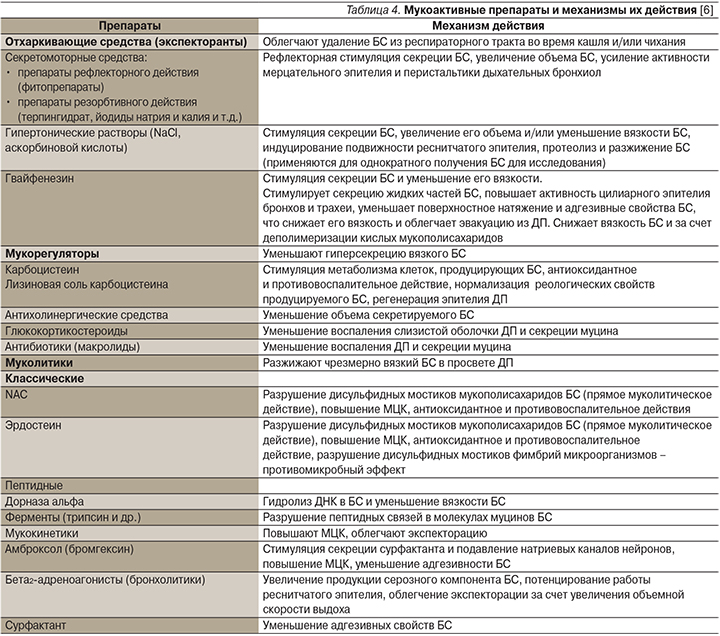
Отхаркивающая (прокашлевая) терапия показана в случаях, когда кашель выполняет полезную защитную функцию и его необходимо стимулировать (например, при ХОБЛ, бронхоэктазах, муковисцидозе).
Показанием к применению экспекторантов (секретомоторных препаратов) [8, 9] является продуктивный кашель с незначительными затруднениями экспекторации мокроты при заболеваниях НДП (бронхиты острые и хронические, бронхоэктатическая болезнь, пневмония и др.). Назначение экспекторантов при непродуктивном (сухом) кашле может приводить к его усилению.
Необходимо отметить, что растительное происхождение лекарственного средства еще не означает полной безопасности его применения. Так, например, препараты ипекакуаны и термопсиса, способствуя значительному увеличению объема БС, усиливают позывы на рвоту; анис, солодка и душица, обладают довольно выраженным слабительным эффектом. Нужно соблюдать особую осторожность при применении фитопрепаратов у детей раннего возраста с высоким риском рвоты и аспирации.
В то же время по своей ценности указанные средства лишь незначительно превосходят плацебо, особенно в рекомендуемых дозах. Для эффективного воздействия этих препаратов на экспекторацию мокроты требуется назначение их в дозах, близких к рвотным (например, отвары по 1 столовой ложке не менее 6 раз в день). Это затрудняет лечение больных, т.к. в случае применения данных средств возникает необходимость разведения во времени их приема с приемом пищи не менее чем на 2 часа.
Практически все фитопрепараты активны только перорально, поэтому ингаляционное их введение может оказывать в лучшем случае психотерапевтическое действие. Учитывая недостатки лекарственных форм, приготовленных из растительного сырья в домашних условиях, предпочтительнее применять профессионально приготовленные официнальные средства.
Одновременное применение экспекторантов с противокашлевыми средствами приводит к скоплению БС в ДП, провоцируя вторичное инфицирование.
В противоположность экспекторантам мукорегуляторы, в первую очередь карбоцистеин и его лизиновая соль [8, 9], не вызывают значительного увеличения объема БС в ДП. Препараты обладают одновременно мукорегулирующим и муколитическим эффектами. Кроме того, карбоцестеин является мощным прямым и непрямым антиоксидантом. Под его воздействием происходят регенерация слизистой оболочки ДП, восстановление ее структуры, уменьшение (нормализация) количества бокаловидных клеток, особенно в терминальных бронхиолах, а значит, и уменьшение количества вырабатываемого БС.
Противовоспалительное мукорегенераторное муколитическое действия препарата потенциально полезны во всех случаях развития острых ринитов, риносинуситов, трахеитов, бронхитов, отитов. Карбоцистеин одинаково эффективен во всех участках ВЛП и НДП, в полости среднего уха, где имеет место сходное строение псевдомногорядного реснитчатого эпителия.
При назначении карбоцистеина объем мокроты в среднем увеличивается к 3-му дню, в течение последующих 2–3 дней мокрота становится заметно менее вязкой и легче откашливается. Хороший и стабильный муколитический эффект отмечается к 7–9-м суткам лечения. Добавление лизина к молекуле карбоцистеина повысило эффективность препарата: отмечена возможность его отмены после 4 дней приема (при ОРВИ), при этом в течение 8 дней после прекращения приема сохраняются усиление МЦК и нормальная вязкость БС (т.н. постмукоактивный эффект).
Карбоцистеин эффективен только при приеме внутрь, поэтому его препараты выпускаются только в пероральных лекарственных формах – таблетках, капсулах, сиропах. Может применяться и у детей, начиная с 5-летнего возраста, для них разработаны специальные лекарственные формы – сиропы для детей.
Классический муколитик N-ацетил-L-цистеин (NAC) [8, 9] относится к группе тиолов. В результате деполимеризации макромолекул мокрота, в т.ч. гнойная, становится менее вязкой и адгезивной. В то же время NAC является мощным антиоксидантом, оказывающим как прямое, так и непрямое действие даже в очень низких концентрациях. В связи с тем что NAC является предшественником глутатиона (принимающего участие в процессах детоксикации) он широко используется и при лечении передозировки парацетамола. Антиоксидантное действие NAC косвенно влияет на продукцию БС, т.е. он оказывает мукорегуляторный эффект.
NAC одинаково эффективен при пероральном и парентеральном, в т.ч. ингаляционном и внутрибронхиальном, введении. Многообразие лекарственных форм NAC: таблетки, порошки, растворы, ампулы для инъекций – позволяет варьировать пути введения и индивидуализировать терапию. Препарат применяется в средней суточной дозе 600 мг. Действие NAC после приема внутрь начинается через 30–90 минут. Этому способствует и его выпуск в виде шипучих таблеток и порошков для однократного приема в сутки, что ускоряет всасывание в желудочно-кишечном тракте. Следует отметить, что пероральный прием NAC может инактивировать действие антибиотиков, принятых внутрь. Возможность однократного приема обоих препаратов позволяет развести время их приема на 2 часа. Мощный муколитический эффект NAC может привести к т.н. заболачиванию легких, особенно при сниженном кашлевом рефлексе, поэтому его применение нежелательно маленькими детьми и лицами старших возрастных групп.
NAC хорошо переносится в пероральных и инъекционных формах, однако его ингаляции могут вызывать бронхиальную обструкцию у больных БА и ХОБЛ. В этих случаях возможно введение в раствор NAC для ингаляций растворов фенотерола или ипратропия бромида. Из редких нежелательных явлений отмечаются нерезко выраженные диспепсические расстройства.
Широко распространенный мукокинетик бромгексин [8, 9] является пролекарством. При приеме внутрь препарат в печени превращается в активный метаболит – амброксол. Действие препарата начинается через 24–48 часов после перорального приема. Отличительными особенностями бромгексина являются его самостоятельное противокашлевое действие и способность провоцировать бронхиальную обструкцию. Эти нежелательные явления отмечаются при использовании эффективных доз (8–12–16 мг на прием 3 раза в день), что заметно ограничивает прием препарата. Для преодоления нежелательного действия бромгексина рекомендуется применять его только в виде комбинированных препаратов.
Самым важным свойством амброксола является его способность стимулировать синтез сурфактанта альвеолярными пневмоцитами II порядка и клетками Клара, тем самым восстанавливать МЦК. Сурфактанкт помогает восстановлению двухфазности БС – разделению вязкого секрета на золь и гель. Уменьшение адгезивности БС, облегчение работы мерцательного эпителия повышают МЦК. Кроме того, препарат стимулирует образование трахеобронхиального секрета пониженной вязкости и оказывает умеренное секретолитическое действие. Таким образом, амброксол разжижает вязкий, липкий БС, уменьшает его адгезивность, обеспечивает продвижение секрета по ДП и выраженный отхаркивающий эффект. Способность амброксола повышать синтез, секрецию сурфактанта и блокировать его распад делает целесообразным его применение больными, находящимися на длительной ингаляционной терапии, в частности оксигенотерапии (при которой разрушается сурфактант) или искусственной вентиляции легких.
Амброксол эффективен при назначении внутрь и парентерально, в т.ч. в ингаляциях. Его широкому применению способствует и большое разнообразие лекарственных форм (таблетки, капсулы, растворы для приема внутрь, ингаляций и внутривенного введения). Очень удобно наличие капсул ретард, позволяющих принимать препарат 1 раз в день. После первого приема амбраксола внутрь действие начинается через 24–72 часа. В случае необходимости быстрого разжижения чрезмерно вязкой мокроты одновременно с пероральным назначением препарата возможно начать его ингаляционное введение (№ 5–6).
Известно, что амброксол проникает через плацентарный барьер и выделяется с грудным молоком, поэтому не рекомендуется назначать препарат в I триместре беременности и при кормлении грудью, хотя тератогенный эффект не описан. В то же время способность амброксола потенцировать синтез сурфактанта применяется при лечении и/или профилактике дистресс-синдрома новорожденных. В таких случаях препарат может назначаться матери в последнем триместре беременности и/или во время кормления грудью либо непосредственно новорожденным в педиатрических дозах.
Возможности выбора мукоактивных препаратов отражены в табл. 5.
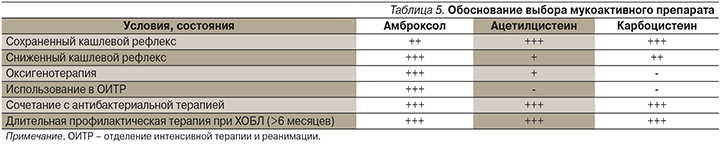
Противокашлевая терапия
Классификация противокашлевых препаратов представлена на рис. 1.
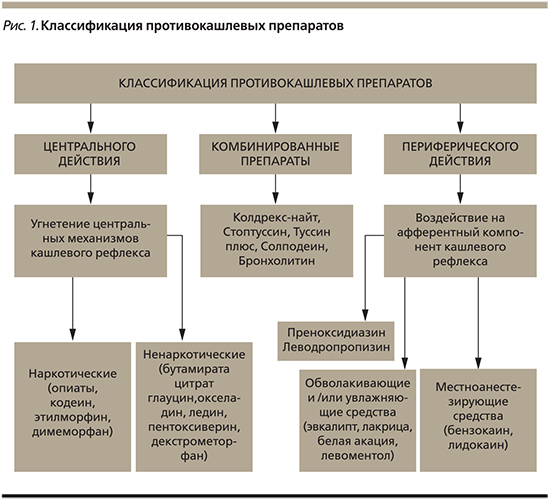
Показаниями к проведению противокашлевой терапии являются заболевания и состояния, сопровождающиеся жалобами на сухой кашель, кашель раздражения, бесполезный, непродуктивный, часто болезненный, не способствующий очистке ДП:
- воспалительные заболевания ВДП и НДП (острый и хронический ларингит, фарингит, трахеит, бронхит) – преимущественно препараты местного действия – обволакивающие и/или увлажняющие средства (эвкалипт, лакрица, белая акация, левоментол);
- заболевания плевры (сухой плеврит, новообразования плевры);
- раздражение возвратного нерва в средостении (лимфома, увеличенные лимфатические узлы, опухоль);
- давление на трахею и бронхи (тиреоидит, аневризма аорты, опухоль);
- милиарный туберкулез легких;
- коклюш;
- заболевания сердечно-сосудистой системы – «сердечный» кашель как аура приступа сердечной астмы;
- рефлекторный кашель при раздражении нервных окончаний n. vagus при заболеваниях уха, печени, желчного пузыря, кишечника, желудка (в послеоперационном периоде после хирургических вмешательств).
Специфическая противокашлевая терапия является этиотропной или патогенетической (например, при ГЭРБ, КСВДП, КВБА). Неспецифическая противокашлевая терапия является скорее симптоматической. Ей принадлежит ограниченная роль вследствие высокой вероятности определения истинной причины кашля и назначения специфического лечения. Такая терапия показана преимущественно в случаях, когда спецфическая терапия не будет успешной, например, при неоперабельном раке легкого.
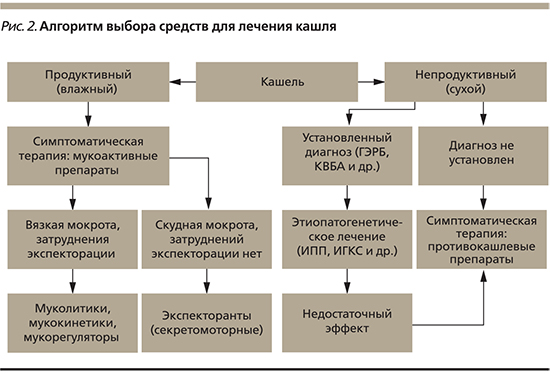
Таким образом, очевидно, что кашель – это только симптом какого-либо заболевания, нередко тяжелого. Поэтому лечение только кашля, без попытки выяснения причины его развития, некорректно. Успех терапии кашля во многом зависит от правильной диагностики и назначения соответствующей терапии. При установленной причине заболевания в первую очередь должно проводиться этиотропное и патогенетическое лечение основного заболевания. Параллельно может проводиться симптоматическое медикаментозное лечение кашля, которое является либо противокашлевым – для предотвращения, управления и подавления кашля, либо отхаркивающим (прокашлевым) – для большей эффективности кашля (рис. 2).


