Многообразие этиологических факторов и патогенетических механизмов, участвующих в развитии нарушений мозгового кровообращения (НМК), определяет сложность выбора терапии. В то же время независимо от причин, вызывающих ишемию мозга, пути реагирования его метаболизма на ишемию универсальны [1].
Мозг человека, на долю которого приходится 2% от общей массы тела, утилизирует 95% всего потребляемого кислорода, при этом интенсивность потребления его нейронами в десятки и сотни раз превышает таковую в клетках других тканей и органов (350–450 мкл кислорода на 1 г ткани мозга в 1 минуту). Мембраны нейронов характеризуются высоким содержанием арахидоновой и докозагексаеновой кислот, окисляющихся под действием активных форм кислорода [2].
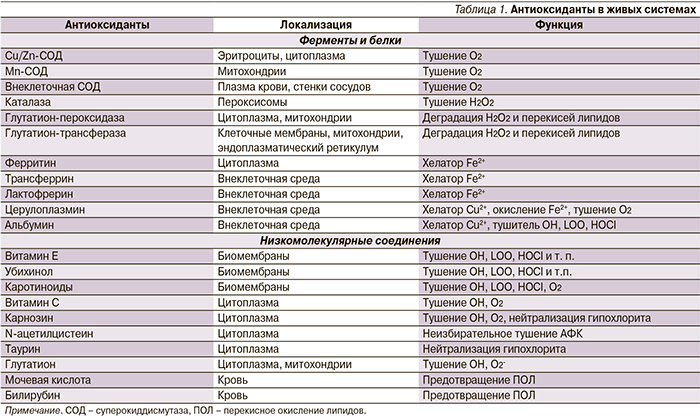
В нормальных физиологических условиях содержание высокореакционных кислородных радикалов уравновешивается эндогенной антиоксидантной системой. В ее состав входят как ферменты, так и многочисленные низкомолекулярные антиоксиданты или соединения, препятствующие образованию свободных радикалов (табл. 1) [2].
Нарушения кровоснабжения мозга инициируют каскад метаболических нарушений, среди которых ключевое место занимают реакции свободнорадикального окисления белков, нуклеиновых кислот и липидов активными формами кислорода (АФК). Накопление высокотоксичных продуктов окисления оказывает системное воздействие не только на клеточные мембраны, но и на нейроны в целом, приводя их к гибели [3, 4].
Окисление мембранных фосфолипидов, которые содержат ненасыщенные жирнокислотные остатки, происходит по цепному механизму. Эти процессы приводят к быстрому нарушению целостности клеточных мембран, не совместимому с жизнеспособностью клетки. Молекулярными продуктами окисления фосфолипидов являются гидропероксиды жирных кислот, а также соединения альдегидной природы – гидроксиноненали и малоновый диальдегид. При нормальных условиях функционирования концентрация этих соединений в тканях мала, но в условиях нарушения клеточного метаболизма создается ситуация, характеризующаяся повышенной продукцией АФК и носящая название окислительного стресса [1–4].
Процессы деструкции белков и нуклеиновых кислот под действием АФК могут происходить параллельно с деструкцией мембранных липидов. В окислительную модификацию белков вовлекаются различные аминокислотные радикалы. Амино- и сульфгидрильные группы белков особенно легко окисляются АФК и гипохлоритом. Этот вид модификации является, как правило, обратимым и зависит от энергетического потенциала клетки и наличия в ней восстановленных форм глутатиона, цистеина, тиоредоксина. Окисление белков может приводить к нарушению и модификации их функции. Так, влияние АФК на Na/K-АТФазу вызывает утрату чувствительности фермента к регулирующему действию АТФ; окислительная атака SH-групп NMDA-рецепторов приводит к подавлению их функции, что отражает контроль за экзайтотоксическими эффектами глутамата со стороны АФК. Фермент ксантиндегидрогеназа модифицируется в условиях окислительного стресса двумя различными способами. Она превращается в ксантиноксидазу и начинает продуцировать супероксид-анион, что приводит к увеличению внутриклеточного уровня АФК [2, 5].
Кроме цистеина в белковых молекулах легко окисляются лизин, тирозин и карбоксильные группы дикарбоновых аминокислот. В ходе разнообразных реакций накапливаются орто- и метатирозин, метионинсульфоксид, а также разнообразные карбонильные производные белков. Белки легко взаимодействуют с сахарами, что приводит к накоплению гликированных продуктов. Гликирование белков обычно осуществляется в результате прямого взаимодействия сахаров с аминогруппами лизина (наиболее легко гликируются те радикалы лизина, соседней группой которых является пролин). В результате образуются Шиффовы основания, которые при перегруппировке превращаются в стабильные соединения (продукты Амадори). Вместе с продуктами ПОЛ они накапливаются в липофусциновых гранулах, образующихся в нейронах. Радикальная атака нуклеиновых оснований в ДНК и РНК приводит к гидроксилированию и нарушает регулярную упаковку двойной спирали ДНК или стабильность РНК. Это вызывает фрагментацию молекул нуклеиновых кислот – дефекты, которые с трудом поддаются репарации [5].
Разработка проблемы защиты мозга от ишемии стала приоритетным направлением современной ангионеврологии.
Милдронат (3-(2,2,2-триметилгидразиний) пропионата дигидрат) является конкурентным ингибитором γ-бутиробетаингидроксилазы. Действие Милдроната обусловлено его антиоксидантным и мембранопротекторным эффектами, которые обеспечиваются следующими путями [6]:
- Ингибирует свободнорадикальное окисление липидов клеточных мембран, стабилизирует клеточные мембраны.
- Повышает активность антиоксидантных ферментов, в частности СОД.
- Ингибирует свободнорадикальную стадию синтеза простагландинов.
Материал и методы исследования
Под наблюдением находились 67 больных в возрасте от 45 до 76 лет, страдающих артериальной гипертензией в сочетании с атеросклерозом. Длительность повышения артериального давления (АД) у больных составила ≥10 лет.

Диагностика формы и стадии цереброваскулярного заболевания и основного сосудистого процесса проводилась с использованием общеклинических методов, неврологического осмотра, а также магнитно-резонансной томографии (МРТ) головы, дуплексного сканирования магистральных артерий головы, суточного мониторирования АД, офтальмологического обследования, ЭКГ, Эхо-КГ, исследования гемореологических показателей.
У всех больных была диагностирована дисциркуляторная энцефалопатия (ДЭ) II стадии без предшествующих НМК (45 больных) или с эпизодами повторных НМК – ишемических инсультов (ИИ) в анамнезе (22 больных).
Множественные очаговые и диффузные изменения головного мозга у больных с ДЭ II стадии были подтверждены при МРТ головного мозга. Локализация ИИ у 18 пациентов соответствовала бассейну кровоснабжения средней мозговой артерией, у 4 – бассейну артерий вертебрально-базилярной системы. По патогенетическому подтипу больные, перенесшие ИИ, распределились следующим образом: лакунарный инсульт – 9, кардиогенный эмболический инсульт – 6, атеротромботический инсульт – 5, гемодинамический инсульт – 2.
При ДЭ II ст. без предшествующих НМК отмечена большая выраженность как субъективных, так и объективных симптомов заболевания.
Признаки декомпенсации хронических НМК включали снижение психической и физической активности, апатию, учащение приступов головной боли и головокружения, жалобы на общую слабость, быструю утомляемость и истощаемость при выполнении привычной работы, трудности концентрации, своевременного переключения внимания, организации своей деятельности, снижение памяти и работоспособности, раздражительность и эмоциональную лабильность.
В неврологическом статусе выявлялись асимметрия носогубных складок, девиация языка, анизорефлексия, вестибуломозжечковые (головокружение, неустойчивость), псевдобульбарные («насильственный» смех и плач) и экстрапирамидные нарушения (тремор головы и пальцев рук, гипомимия, ригидность мышц, замедленность движений), снижение интеллектуально-мнестических функций.
У больных с последствиями НМК в клинической картине превалировали двигательные нарушения от легкого монопареза руки до выраженного гемипареза (у 17 больных), расстройства статики и координации (у 5 больных) и легкие нарушения корковых функций (у 11 больных). Астенический и астенодепрессивный синдромы имели место у 9 больных.
По клиническим синдромам больные с последствиями НМК распределились следующим образом (табл. 2).
Милдронат вводили ежедневно в течение 20 дней внутривенно капельно в дозе 5 мл 10%-ного раствора (т.е. 500 мг) в 200 мл 0,85%-ного раствора хлорида натрия. Все пациенты получали антиагреганты и статины. При необходимости назначались антигипертензивные, кардиальные препараты и антикоагулянты. Пациенты получали подобранную антигипертензивную терапию, не изменявшуюся во время проведения исследования.
Все больные с последствиями НМК получали Милдронат в сроки до года после НМК.
Оценка эффективности лечения основывалась на субъективной оценке основных симптомов заболевания (головная боль, головокружение, шум в голове, нарушение сна, утомляемость, снижение памяти, депрессия и тревожность, эмоциональная лабильность) с использованием 5-балльной рейтинговой шкалы. Оценка выраженности каждого симптома была стандартизирована (от «0» – нет нарушений, до «4» –значительно выраженные проявления). Исследование неврологического статуса включало оценку двигательных, вестибуло-мозжечковых, экстрапирамидных, чувствительных, псевдобульбарных и речевых нарушений. Эффект лечения исследователь и больной оценивали по 5-ступенчатой шкале «отлично», «хорошо», «удовлетворительно», «неудовлетворительно», «отсутствие эффекта».
 Влияние Милдроната на когнитивные нарушения у больных с ДЭ II стадии без нарушений высших корковых функций изучалось при помощи нейропсихологического исследования.
Влияние Милдроната на когнитивные нарушения у больных с ДЭ II стадии без нарушений высших корковых функций изучалось при помощи нейропсихологического исследования.
Нейропсихологическое исследование включало:
1) Общую оценку динамики психической деятельности с регистрацией:
- общего времени выполнения задания;
- времени запоминания 10 слов;
- времени выполнения серийного счета «100-7».
2) Исследование слухо-речевой памяти:
- запоминание 10 слов после 5-кратного повторения с последующими двумя отсроченными воспроизведениями;
- воспроизведение числовых рядов в прямом (кратковременная память) и обратном (оперативная память) порядках.
3) Исследование зрительной памяти: тест Бентона – запоминание и графическое воспроизведение 10 последовательно предъявленных картинок с учетом количества правильных ответов и количества ошибок.
4) Исследование интеллектуальной деятельности: выполнение серийных счетных операций «100-7» с оценкой времени выполнения теста и количества ошибок.
5) Исследование внимания: поиск чисел по таблицам Шульте с оценкой времени выполнения задания.
При наличии у больных афазии и других нарушений высших корковых функций очагового типа проводилось нейропсихологическое исследование речевых функций, письма, чтения, счета, гнозиса и праксиса с использованием набора стандартизованных нейропсихологических проб.
У всех больных оценивалось состояние их эмоционально-волевой сферы, общей двигательной и психической активности.
Состояние процессов ПОЛ оценивали по ряду информативных кинетических параметров Fe2+-индуцированной хемилюминесценции (ХЛ) суммарной фракции липопротеидов низкой и очень низкой плотности сыворотки крови, выделяемых в системе хлористого кальция с гепарином и используемых в качестве липидного субстрата окисления [7]. Измерения Fe2+-индуцированной ХЛ проводили на люминометре-1251, LKB, Швеция. В работе анализировали следующие параметры ХЛ: амплитуду быстрой вспышки h (мВ), отражающую уровень предобразованных продуктов ПОЛ (преимущественно гидроперекисей липидов); устойчивость липопротеиновых структур к окислению τ (с), отражающую эффективность антиоксидантной защиты; интенсивность медленной фазы Н (мВ), характеризующую максимальную способность липидов к перекисному окислению.
Статистическая обработка полученных результатов проводилась на основе пакета программ STATISTICA 99 (StatSoft, США).
Результаты исследования и их обсуждение
I. Переносимость лечения
Побочные эффекты на фоне курса лечения были зарегистрированы у 7 больных и выражались преимущественно в усилении колебаний АД (n=6) и болях в области сердца (n=1). При этом связь возникших побочных эффектов с проводимой терапией была оценена лечащим врачом как «неизвестная».
II. Клиническая эффективность лечения
Динамика субъективных клинических симптомов. Улучшение общего состояния наступило у 50 (74,6%) больных. Уже на второй неделе лечения у пациентов увеличивался интерес к окружающему, уменьшались признаки психической истощаемости, исчезала сонливость в дневные часы, упорядочивалось поведение и психоэмоциональные реакции. Уменьшались неприятные субъективные ощущения в области головы.
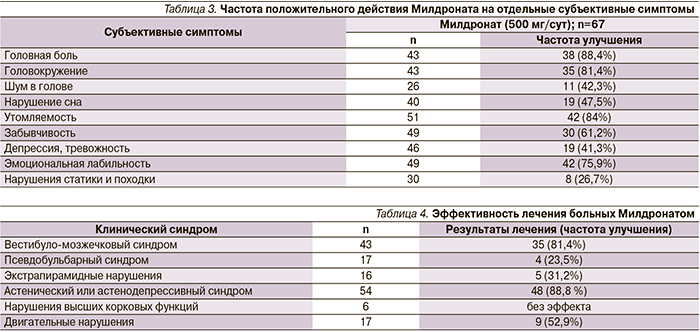
Сопоставление балльной оценки тяжести клинического синдрома до начала исследования и по его завершении (спустя 20 дней) выявило статистически значимое улучшение состояния больных по таким клиническим симптомам, как головная боль, головокружение, утомляемость, забывчивость, эмоциональная лабильность (табл. 3, 4).
Результаты нейропсихологического исследования. Для оценки влияния терапии Милдронатом на психические процессы 56 больным было проведено психологическое исследование.
У всех больных до начала лечения выявлялись те или иные нарушения когнитивных функций, из которых ведущими были нарушения зрительной памяти, интеллектуальной деятельности и внимания.
На фоне лечения Милдронатом улучшилась общая психическая деятельность, что выражалось в виде уменьшения времени выполнения задания и укорочения времени запоминания 10 слов.
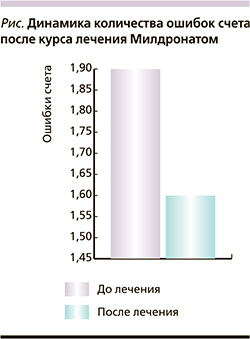
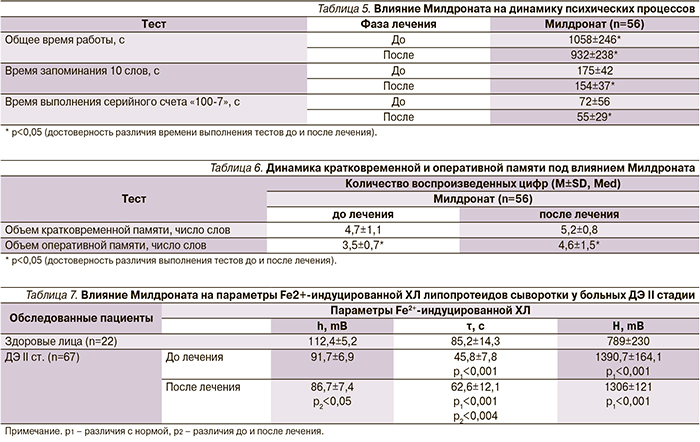
Исследование интеллектуальной деятельности выявило статистически значимое укорочение времени выполнения задания (табл. 5) и уменьшение числа допускаемых ошибок (см. рисунок).
Изменений кратковременной памяти (воспроизведение числовых рядов в прямом порядке) после курса лечения Милдронатом зарегистрировано не было. Улучшение же оперативной памяти (воспроизведение числовых рядов в обратном порядке), где значительно возрастает роль процессов внимания, было статистически значимым (табл. 6).
Исследование зрительной памяти при помощи теста Бентона после проведенного курса лечения показало достоверное уменьшение количества ошибок и увеличение числа правильных ответов.
При исследовании слухо-речевой памяти путем запоминания 10 слов после 5 повторов и внимания при помощи поиска чисел по таблицам Шульте существенной динамики показателей не получено.
Таким образом, результаты нейропсихологического исследования дают основание предположить, что терапия Милдронатом оказывает определенное положительное влияние на протекание психических процессов у больных ДЭ II стадии. Следует отметить, что Милдронат оказывал влияние на темп или «скоростные характеристики» психической деятельности в виде укорочения времени выполнения задания и серийного счета, а также на процессы, связанные с интеллектуальной деятельностью (проба с вычитанием «100-7»), вниманием (запоминание ряда цифр в обратном порядке) и зрительной памятью.
Заключительная оценка эффективности лечения врачом и пациентом. После курса лечения врач и больной выносили субъективную заключительную оценку эффективности лечения в соответствии с представленной в протоколе исследования 5-ступенчатой шкалой. В большинстве случаев были получен положительные оценки, количество больных, оценивших результаты терапии как «отлично», было 7%; доли субъективных оценок «хорошо» и «удовлетворительно» составили 17,9 и 44,8%.
Динамика процессов ПОЛ у больных ДЭ II стадии под влиянием Милдроната
Результаты исследования показали, что у больных ДЭ II cтадии изменения параметров ПОЛ до начала лечения Милдронатом касались увеличения способности липопротеидных структур к окислению, повышения радикалообразования и снижения резистентности липопротеидов к окислению. Лечение Милдронатом в течение 20 дней приводит к увеличению длительности латентного периода ХЛ (τ), отражающего резистентность липопротеидов к ПОЛ. После курса лечения у больных, получавших Милдронат, также произошло статистически значимое снижение уровня гидроперекисей липидов (табл. 7).
Исходя из результатов настоящего исследования, стабилизация липопротеидных компонентов крови к перекисному окислению, проявившаяся в увеличении их антиоксидантного статуса под влиянием Милдроната, может быть объяснена наличием антиоксидантных свойств у этого препарата. Возможно, для достижения более эффективного терапевтического результата следует в дальнейших исследованиях увеличить суточную дозу Милдроната.
Таким образом, лечение Милд-ронатом (500 мг ежедневно) приводило к повышению резистентности липопротеидов сыворотки крови пациентов к перекисному окислению, что свидетельствует о способности препарата осуществлять антиоксидантную защиту липопротеидов.
Анализируя результаты лечения больных, можно констатировать, что отличные, хорошие и удовлетворительные результаты лечения наблюдались у 69,7% пациентов с ДЭ II ст.
Наиболее благоприятный эффект отмечен у больных с неустойчивостью настроения, нарушениями эмоционально-волевой сферы, памяти и способности концентрации внимания, т.е. в тех случаях, когда имело место диффузное снижение корковой активности. У этих пациентов под влиянием лечения уменьшалась лабильность эмоционально-волевой сферы, исчезала тревожность, заметно преобладала положительная окраска эмоциональных переживаний, улучшались способность концентрации внимания и память, больные становились активнее. Довольно хороший эффект наблюдался и у пациентов с головными болями, которые к концу лечения резко уменьшались по интенсивности и становились более редкими.
В результате исследования было установлено, что у больных с последствиями НМК Милдронат оказывает положительное влияние в основном на их общее состояние и меньшее на очаговые неврологические симптомы. У пациентов с нарушениями корковых функций за счет очаговых выпадений (афазия, алексия, аграфия, акалькулия, агнозия) эффективность Милдроната была ниже, чем при симптомах диффузного коркового поражения. У них улучшался прежде всего нейродинамический фон: повышалась концентрация внимания, его устойчивость, способность к переключениям, уменьшалась истощаемость. Степень восстановления нарушенных очаговых корковых функций определялась в значительной мере тяжестью поражения. Значительно меньший эффект наблюдался при лечении Милдронатом больных с выраженными двигательными нарушениями. В этих случаях значительного улучшения двигательных функций не наблюдалось. Однако можно было отметить ускорение восстановления этих функций. Умеренное улучшение двигательных функций наблюдалось у 9 больных с постинсультными гемипарезами и выражалось в основном в улучшении функции ходьбы, навыков самообслуживания и увеличении общей двигательной активности. Применение Милдроната , по-видимому, привелоих к мобилизации скрытых ранее возможностей. В 5 наблюдениях в период лечения Милдронатом уменьшилась выраженность тремора статического напряжения, у 2 пациентов уменьшилась мышечная ригидность и замедленность движений.
При объяснении эффективности лечения больных хроническими НМК мы принимали во внимание тот факт, что степень восстановления нарушенных функций зависит не только от давности и величины очага, но и от его локализации. Так, концентрация двигательных путей в колене внутренней капсулы определяет плохой прогноз для обратного развития симптомов при локализации очаговых изменений в этой области. Напротив, сложность организации мнестических функций, складывающихся из координированной работы многих отделов мозга, дает надежду на успех за счет мобилизации и компенсаторной деятельности различных звеньев под влиянием лечения.
Известно, что для осуществления любого вида психической деятельности необходим ряд факторов: определенные оптимальный тонус коры и сила корковых процессов (т.е. их концентрированность, уравновешенность, подвижность), сохранность первичных и ассоциативных корковых зон, регуляция и контроль сознательной деятельности.
Следует отметить, что положительные результаты лечения Милдронатом больных с органическими заболеваниями нервной системы в определенной степени следует объяснять повышением целеустремленности, собранности пациентов, уменьшением их истощаемости, улучшением внимания и памяти.
У 9 больных с последствиями НМК наблюдались двигательные нарушения в сочетании с астенодепрессивным или астеническим синдромом. Для этой группы пациентов было характерно сочетание пониженного фона настроения со снижением уровня активности, развивающегося на фоне повышенной утомляемости, истощаемости, не способности к длительному психическому и физическому напряжению. У многих больных наряду с астенией и депрессией отмечалось наличие ипохондрических реакций. Улучшение общего состояния на фоне лечения Милдронатом наблюдалось у всех больных этой группы: у 8 пациентов улучшение было значительным. Оно выражалось в том, что больные в процессе лечения Милдронатом становились активнее, более собранными, у них исчезала тревожность, подавленность настроения, повышался общий фон настроения, нарастала скорость реакций, улучшались внимание, его устойчивость и переключаемость, уменьшалась аспонтанность.
Результаты клинико-биохимического исследования, представленные в данной работе, указывают на значимость свободнорадикальных процессов липидного окисления в патогенезе сосудистых заболеваний головного мозга. При хронических нарушениях мозгового кровообращения в условиях окислительного стресса, поэтому антиоксидантная система мозга не способна осуществлять полноценную защиту от свободнорадикальной атаки, становится очевидной необходимость усиления антиоксидантной защиты, которая может быть опосредована природными или нетоксичными синтетическими антиоксидантами.
Таким образом, применение Милдроната имеет значение в компенсации имеющихся у больных ДЭ проявлений дисфункции мозга, восстановления физической и психической активности.
Выводы
У большинства больных ДЭ II ст. на фоне лечения Милдронатом произошло улучшение со стороны как субъективной, так и объективной неврологической симптоматики, причем наиболее четкую динамику претерпели такие синдромы заболевания, как кохлеовестибулярный, астеноневротический и цефалгический.
Получено подтверждение экспериментальных данных об антиоксидантном действии Милдроната, которое реализуется путем повышения эндогенного антиоксидантного статуса организма.
Выявлено положительное влияние Милдроната на когнитивные функции больных ДЭ II ст. по данным нейропсихологического исследования, что позволяет говорить о нейротрофическом действии препарата.
Препарат Милдронат может быть рекомендован к применению в комплексной терапии больных с хроническими цереброваскулярными заболеваниями.


